
Les meilleurs professeurs de Physique - Chimie disponibles

5 (605 avis)

1er cours offert !

5 (388 avis)

1er cours offert !

4,9 (187 avis)

1er cours offert !

5 (275 avis)

1er cours offert !

5 (412 avis)

1er cours offert !

5 (263 avis)

1er cours offert !

4,9 (153 avis)

1er cours offert !

4,9 (115 avis)

1er cours offert !

5 (605 avis)

1er cours offert !

5 (388 avis)

1er cours offert !

4,9 (187 avis)

1er cours offert !

5 (275 avis)

1er cours offert !

5 (412 avis)

1er cours offert !

5 (263 avis)

1er cours offert !

4,9 (153 avis)

1er cours offert !

4,9 (115 avis)

1er cours offert !
C'est parti
I. A partir de la masse du produit
La quantité de matière de l'espèce X est donnée par la relation:
| | 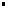 n(X): quantité de matière de l'espèce X en mol n(X): quantité de matière de l'espèce X en mol
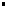 m(X): masse de l'espèce X en kg ou en g m(X): masse de l'espèce X en kg ou en g
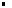 M(X): masse molaire de l'espèce X en kg.mol-1 ou en g.mol-1 M(X): masse molaire de l'espèce X en kg.mol-1 ou en g.mol-1 |
Remarques:
- Si l'espèce X est atomique, M(X) est donnée dans le tableau périodique des éléments.
- Si l'espèces X est moléculaire, M(X) doit être calculée à partir des données du tableau périodique des éléments en effectuant la somme des masses molaires atomiques de tous les atomes constituant la molécule.
- Si l'espèce (X) est un solide ionique, M(X) doit être calculée à partir des données du tableau périodique des éléments en effectuant la somme des masses molaires atomiques des éléments figurant dans la formule statistique de X.
II. A partir du volume d'un liquide
1. Masse volumique.
La masse volumique d'un corps est la masse de l'unité de volume de ce corps et se calcule en effectuant le rapport entre sa masse et son volume.
| | 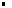 µ(X): masse volumique du corps X en kg.m-3 ou en g.cm-3 µ(X): masse volumique du corps X en kg.m-3 ou en g.cm-3
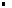 m(X): masse du corps X en kg ou en g m(X): masse du corps X en kg ou en g
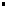 V(X): volume du corps X en m3 ou en cm3 V(X): volume du corps X en m3 ou en cm3 |
2. Densité d'un liquide.
La densité d'un liquide est le rapport entre la masse d'un certain volume de ce liquide et la masse du même volume d'eau pris dans les mêmes conditions de pression et de température. Cette définition conduit à une expression de la densité qui n'est en générale pas commode à utiliser dans les calculs mais on montre que la densité d'un liquide peut se calculer en effectuant le rapport entre la masse volumique du liquide et la masse volumique de l'eau dans les mêmes conditions de pression et de température.
| | 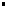 d: densité du liquide d: densité du liquide
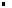 µl: masse volumique du liquide en kg.m-3 ou en g.cm-3 µl: masse volumique du liquide en kg.m-3 ou en g.cm-3
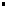 µe: masse volumique de l'eau en kg.m-3 ou en g.cm-3 µe: masse volumique de l'eau en kg.m-3 ou en g.cm-3 |
3. Calcul de la quantité de matière.
La quantité de matière de liquide peut se calculer soit à partir de la masse de liquide, soit à partir de la masse volumique, soit à partir de la densité.
3.1 A partir de la masse.
Il suffit de reprendre la relation donnée au I.
3.2 A partir de la masse volumique.
| | => | m(X)=µ(X).V(X) | or | | . on en déduit: |
| | | | | |
3.3 A partir de la densité.
| | => | µ(X)=µe.d | or | | . on en déduit: |
| | | | | | |
III. A partir de la concentration molaire
1. Concentration molaire.
La concentration molaire d'une espèce X en solution est la quantité de matière de l'espèce X par litre de solution.
| | 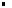 n(X): quantité de matière de l'espèce X en mol n(X): quantité de matière de l'espèce X en mol
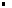 V: volume de la solution en L V: volume de la solution en L
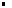 [X]: Concentration de l'espèce X en solution en mol.L-1 [X]: Concentration de l'espèce X en solution en mol.L-1 |
2. Quantité de matière.
D'après ce qui précède:
n(X)=[X].V
IV. A partir du volume d'un gaz
1. A partir de l'équation d'état des gaz parfaits.
| PV=nRT |  P: pression du gaz en Pa P: pression du gaz en Pa
 V: volume du gaz en m-3 V: volume du gaz en m-3
 n: quantité de matière de gaz en mol n: quantité de matière de gaz en mol
 T: température absolue du gaz en K T: température absolue du gaz en K
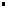 R: constante des gaz parfaits. R=8,32 SI R: constante des gaz parfaits. R=8,32 SI |
2. A partir du volume et du volume molaire.
| | 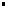 n: quantité de matière de gaz en mol n: quantité de matière de gaz en mol
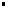 V: volume du gaz V: volume du gaz
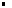 Vm: volume molaire des gaz dans la même unité que V et dans les mêmes conditions de pression et de température Vm: volume molaire des gaz dans la même unité que V et dans les mêmes conditions de pression et de température |
Vous avez aimé cet article ?
Notez-le !

Loading...
Olivier
Professeur en lycée et classe prépa, je vous livre ici quelques conseils utiles à travers mes cours !
























Si vous désirez une aide personnalisée, contactez dès maintenant l’un de nos professeurs !