Chapitres

Le groupe caractéristique carbonyle
Les molécules chimiques organiques comportant au sein de leur composition le groupe carbonyle -CO- sont appelés composés carbonylés. Ce groupe caractéristique est constitué d'un atome d'oxygène et d'un atome de carbone entre lesquels existe une double liaison. Le groupe carbonyle est présent à la fois dans les cétones et les aldéhydes. Sa position permet de distinguer ces deux familles chimiques :
- Dans les aldéhydes le groupe carbonyle est en bout de chaîne, son carbone est lié à un atome d'hydrogène et à un groupe carboné.
- Dans les cétones le groupe carbonyle est inséré entre deux carbones de la chaîne carbonée.

La nomenclature des composés carbonylés
Comment nommer un aldéhyde ?
Le nom d’un aldéhyde est formé en remplaçant la terminaison “e” par le suffixe “al” au nom de l'hydrocarbure correspondant à la chaîne principale. L'atome de carbone du groupe caractéristique carbonyle porte le numéro 1 et n'est pas mentionné.
- Exemple : le butanal
[CH_3-CH_2-CH_2-CHO] Certains composés carbonylés comportent plusieurs groupements caractéristiques carbonyle. Ainsi, on utilise le suffixe “dial” si la molécule possède deux groupements aldéhydes ou “trial” si la molécule possède trois groupes caractéristiques aldéhydes.
- Exemple : le butandial :
[CHO-CH_2-CH_2-CHO]
Comment nommer une cétone ?
Les cétones sont nommées en utilisant le nom de l'alcane ayant la même chaîne carbonée mais en substituant la terminaison "e" par le numéro du carbone portant le groupe carbonyle entre tirets, suivi du suffixe "one".
- Exemple : le butan-2-one :
[CH_3-CO-CH_2-CH_3] 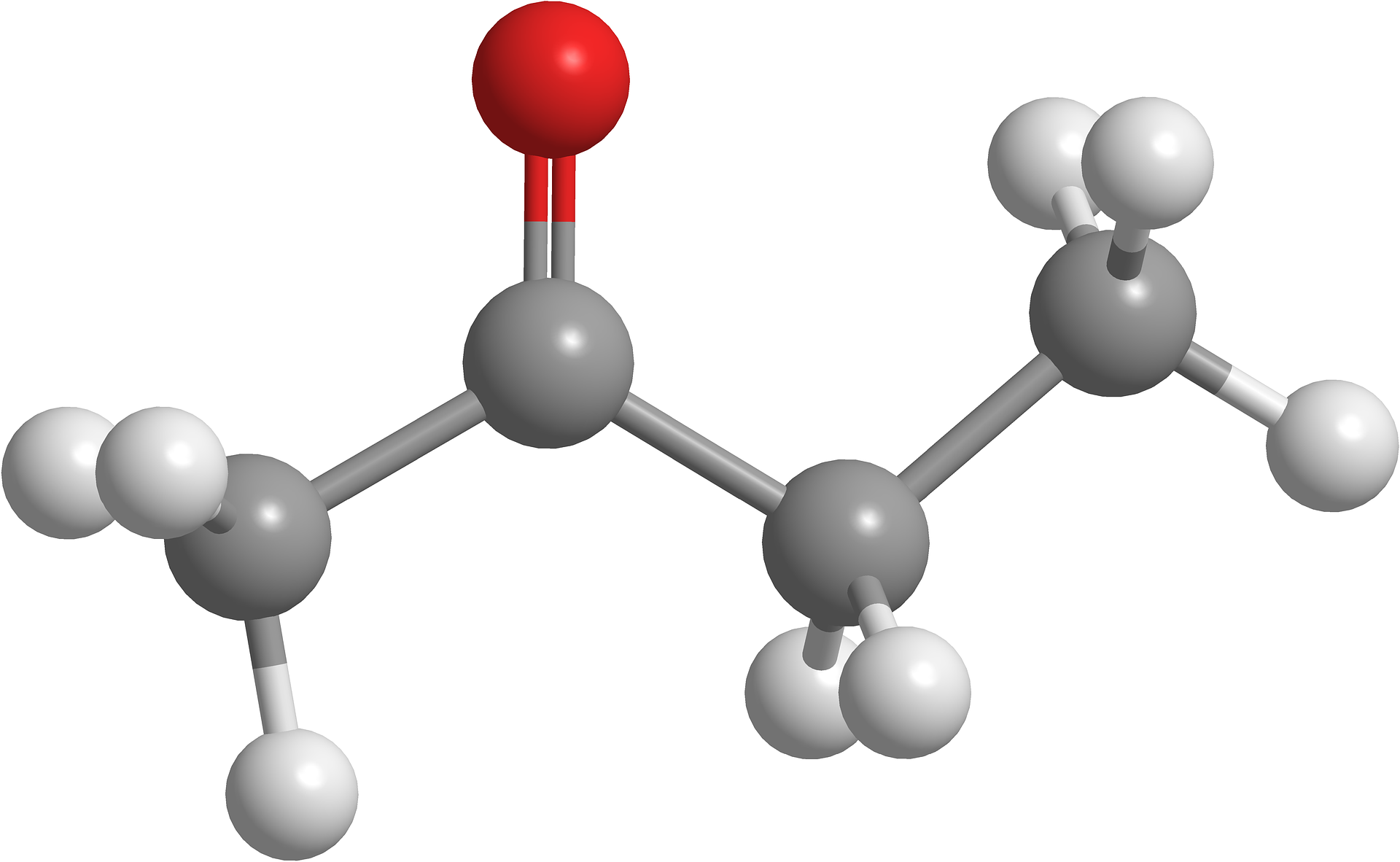
- Exemple : le pentane-2, 4-dione [CH_3-CO-CH_2-CO-CH_3]
Résumé
Tableau récapitulatif des premiers aldéhydes et cétones, en fonction de l’alcane correspondant :
| Nombre d’atomes de carbone | Alcane | Aldéhyde | Cétone |
|---|---|---|---|
| 1 | méthane | méthanal | - |
| 2 | éthane | éthanal | - |
| 3 | propane | propanal | propan-2-one |
| 4 | butane | butanal | butan-2-one |
| 5 | pentane | pentanal | pentan-2-one ou pentan-3-one |
L'oxydation ménagée des aldéhydes et des cétones
C’est par l’oxydation ménagée d’un alcool primaire qu’on obtient un aldéhyde. Si le réactif est en excès, alors l’aldéhyde produit est également oxydé. L'oxydation ménagée d'un aldéhyde conduit à la formation d'un acide carboxylique. Les aldéhydes sont toujours oxydés en acide carboxylique. De nombreux oxydants, même faibles, peuvent amener cette réaction. Par exemple, l'oxygène de l'air oxyde lentement les aldéhydes. C’est pourquoi, même si les flacons contenant des aldéhydes sont bien fermés, il n’est pas rare de constater des quantités non négligeables d’acide carboxylique présentes à cause de l’oxydation. En revanche, les cétones ne peuvent pas subir d’oxydation.
Les propriétés physiques de ces composés carbonylés
Les changements de phase
Les cétones et aldéhydes ont une température d'ébullition plus élevée que les alcanes et les alcènes de même masse molaire. Elle est cela dit moins élevée que pour les alcools : malgré le fait que les molécules contenant les fonctions aldéhydes ou cétones soient polaires, leurs forces intermoléculaires ne sont pas aussi importantes que celles des ponts hydrogènes présents dans les alcools. Voici quelques repères de températures de changement d’état pour les principaux premiers composés des familles aldéhyde et cétone.
| Famille | Composé | Température fusion (°C) | Température d'ébullition (°C) |
|---|---|---|---|
| Aldéhyde | méthanal | -118 | 19 |
| Aldéhyde | éthanal | -123 | 21 |
| Aldéhyde | propanal | -81 | 48 |
| Cétone | propanone | -95 | 56 |
La solubilité des aldéhydes et cétones
Les aldéhydes et cétones sont solubles dans l'eau à condition que leur chaîne carbonée ne soit pas trop longue. Cela s'explique car les fonctions aldéhydes et cétones sont polaires. Lorsque les chaînes carbonées sont trop longues, la solubilité devient difficile du fait de la non polarité des chaînes carbonées longues. En effet, à mesure que la chaîne d'atomes de carbone s’allonge, le caractère hydrophobe de la chaîne carbonée surpasse le caractère hydrophile du groupement carbonyle. Ainsi, plus la chaîne carbonée est longue et plus la volatilité des aldéhydes et cétones se rapproche de celle des alcanes de masses molaires comparables.
Reconnaître les composés carbonylés
Test des composés carbonylés à la 2,4 D.N.P.H.
La molécule 2,4-dinitrophénylhydrazine permet de reconnaître un composés chimique ayant le groupe caractéristique carbonyle. Cette molécule met donc en évidence à la fois les aldéhydes, mais aussi les cétones. Ainsi si on met la solution de D.N.P.H. avec le composé à tester fait apparaître un précipité jaune-orangé, alors le composé testé est bien soit un aldéhyde, soit une cétone.
Test des aldéhydes au réactif de Schiff
Le test de Schiff permet de reconnaître un aldéhyde d’une cétone. En effet, en présence de réactif de Schiff, une solution d’aldéhyde à froid en milieu non basique devient pourpre à violet. En revanche, une solution de cétone ne réagit pas.
Test des aldéhydes à la liqueur de Fehling
La liqueur de Fehling est une solution basique dans laquelle les ions cuivre II sont complexés par le tartrate. En présence de liqueur de Fehling, une solution d’aldéhyde s’oxyde par les ions cuivre et donne un acide carboxylique de couleur rouge brique, caractéristique de la présence d’oxyde de cuivre. Les cétones ne réagissent pas avec ce réactif.
Test des aldéhydes au réactif de Tollens
Le réactif de Tollens est un complexe de nitrate d’argent, mis en solution dans l’ammoniaque. En présence d’un aldéhyde, la solution de Tollens fait apparaître un “miroir d’argent” sur la paroi du tube à essai. Il s’agit en fait d’un dépôt d’argent, produit de l’oxydation de l’aldéhyde par le nitrate d’argent. Là encore, seuls les aldéhydes réagissent. Au contraire, dans une solution avec le réactif de Tollens, les cétones restent telles quelles.
Applications des aldéhydes et des cétones dans la vie courante

Aldéhydes connus
Beaucoup de composants chimiques de la famille des aldéhydes sont utilisés dans la vie quotidienne. En voici une liste non exhaustive :
- Le formaldéhyde ou formol : Il s’agit en fait du méthanal en solution aqueuse. On le retrouve dans de très nombreux produits d’usage courant: mousses isolantes, laques, colles, vernis, encres, résines, papier, produits ménagers, pesticides, bois agglomérés et contreplaqués. Il est également utilisé dans les textiles ainsi que dans certains médicaments et cosmétiques.
- L’éthanal ou acétaldéhyde : Il s’agit d’une molécule chimique très commune. On le trouve en faible quantité notamment dans les feuilles de tabac, dans le romarin, dans le café, dans la menthe ainsi que dans beaucoup d’autres composés et aliments du même genre.
- La vanilline : C’est un aldéhyde aromatique. Ce composé chimique est présent à l’état naturel dans les gousses de vanille et lui donne ce pouvoir odorant. On l’appelle d’ailleurs également vanillaldéhyde ou aldéhyde vanillique.
Cétones connues
Parmi les cétones les plus communes, il faut citer :
- L’acétone C’est l’autre nom plus commun de la propanone. C’est un solvant très utilisé dans l’industrie. On le trouve également dans nos maisons dans les dissolvants pour vernis à ongles par exemple. L’acétone est aussi présente en faible quantité dans le corps humain. On trouve cette substance acide notamment dans le sang et l’urine.
- Le fructose Ce sucre est un isomère du glucose. Sa formule est C6H12O6 et le fructose comporte une fonction cétone. On le trouve à l’état naturel dans les fruits, le miel et même dans le sirop d’agave.























Si vous désirez une aide personnalisée, contactez dès maintenant l’un de nos professeurs !
Superbe…
J’ aime ça, c’est bien structuré
Cet article est cool mais j’aurais aimée que l’on insisté sur la 2,4dnph bref 🎉🎉
Bonjour ! J’aimerais savoir comment obtenir le précipité jaune dans les cétones
Et le précipité rouge dans les Aldéhydes
Bonjour, il nous ferait plaisir de vous aider, n’hésitez pas à contacter nos professeurs sur la plateforme de Superprof. :)
J’ai besoin du soutien en mathématiques, physique, chimie.merçi de m’avoir écouté
Bonjour, il nous ferait plaisir de vous aider. N’hésitez pas à contacter nos professeurs sur la plateforme de Superprof. :)
Can you help me please sister
Je suis un peus nul en physique chimie
Bonjour, pour tout soutien scolaire et quelle que soit la matière, nous vous invitons à contacter nos talentueux professeurs en ligne qui se feront un plaisir de vous aider !