On appelle alcool tout composé organique possédant un groupe hydroxyle – OH lié à un atome de carbone tétragonal. Formule générale d’un alcool : R – OH

Le groupe caractéristique hydroxyle
Le groupement hydroxyle est composé d’un atome d’oxygène lié à un atome d’hydrogène. Lorsque ce groupe caractéristique est lié à un atome de carbone d’une chaîne carbonée aliphatique, alors on parle d’alcool. Même si le groupe caractéristique hydroxyle évoque majoritairement la famille chimique des alcools, on retrouve ce groupe dans différents autres composés chimiques. Par exemple, l’eau (H20) contient un groupe hydroxyle. Le groupe caractéristique hydroxyle apparaît aussi dans la classe de molécule appelée oxyacide : dans certains produits cosmétiques, on trouve des molécules appelées hydroxyde de magnésium ou d’aluminium.
La nomenclature des alcools
On exprime la formule brute d’un alcool de cette manière :
CnH2n+1OH où n est le nombre d’atomes de carbone.
Il est possible que plusieurs groupes caractéristiques hydroxyle (-OH) composent la molécule. Dans ce cas, il ne s’agit plus plus d’un alcool mais d’un polyalcool. Pour nommer un alcool, il est nécessaire de préciser la position du groupe caractéristique hydroxyle dans la chaîne carbonée. Comme pour les alcanes, il faut rechercher la chaîne carbonée la plus longue, c’est-à-dire celle comptant le plus d’atomes de carbones. Le nombre d’atomes de carbone ainsi trouvé donne le préfixe. On coupe ensuite le suffixe “anol” en deux parties séparées par la position du groupe caractéristique -OH :
préfixe + “an” + -position- + ”ol”
Exemple :
- Ici, nous avons 5 atomes de carbone (en noir) et le groupe caractéristique hydroxyle (en rouge) positionné sur le troisième atome de carbone.
- Lorsque 5 atomes de carbone composent la chaîne principale, on utilise le préfixe “pent”.
- En suivant la règle citée ci-dessus, nous obtenons : le pentan-3-ol

Les différentes classes d'alcool
Les alcools sont classés en trois classes :
- primaire,
- secondaire
- et tertiaire.
Pour déterminer à quelle classe un alcool appartient, il convient de repérer le nombre de radicaux organiques liés à l’atome de carbone portant le groupe caractéristique hydroxyle (-OH).
Les alcools primaires
Un alcool primaire se reconnaît par la présence d’un seul radical organique (bien souvent le groupement alkyle) sur l’atome de carbone possédant le groupe caractéristique hydroxyle. On les note ainsi : R-CH2-OH où R est le radical organique Exemple : l’éthanol = CH3-CH2-OH
Les alcools secondaires
Un alcool secondaire se reconnaît par la présence de deux radicaux organiques (R et R’) sur l’atome de carbone possédant le groupe caractéristique hydroxyle. Exemple : le propan-2-ol

Les alcools tertiaires
Un alcool tertiaire se reconnaît par la présence de trois radicaux organiques (R, R’ et R’’) sur l’atome de carbone possédant le groupe caractéristique hydroxyle. Exemple : le 2-méthylpropan-2-ol

La distinction de ces trois classes se justifie par des différences de réactivité.
Les propriétés des alcools
Les alcools sont capables de donner, grâce à leur atome d'oxygène et d’accepter, grâce aux atomes d'hydrogène, des liaisons hydrogènes. Ces liaisons confèrent aux alcools des propriétés physico-chimiques particulières :
Les changements de phase des alcools
Tous les alcools ayant une chaîne carbonée dont le nombre d’atomes de carbone est inférieur à 10 sont des liquides incolores à la température ordinaire. La température d'ébullition des alcools est nettement plus importante que celle des alcanes correspondants. Cette particularité est liée à la présence du groupe hydroxyle.
La solubilité des alcools
La plupart des alcools sont miscibles à l'eau en toutes proportions. Toutefois plus la longueur de la chaîne carbonée est important, moins forte est la solubilité. La molécule d'un alcool possède deux parties : Une partie hydrophobe, la chaîne carbonée. Cette partie ne se lie pas facilement avec l’eau. En revanche, les alcools ont également une partie hydrophile : le groupe hydroxyle qui se lie parfaitement avec les molécules d’eau. Ainsi, on comprend que plus la proportion de la chaîne carbonée est importante (les alcools qui ont beaucoup d’atomes de carbone) et moins la miscibilité est importante. En effet l’importance relative du groupe caractéristique hydroxyle est dans le cas des alcools à longue chaîne carbonée très faible..
L’oxydation ménagée des alcools
Définition
Une oxydation ménagée est une réaction au cours de laquelle la chaîne carbonée du composant organique est conservée. En d’autres termes, à l’issue de la réaction, la chaîne carbonée n’est pas modifiée. Il existe un autre type d’oxydation des alcools : l’oxydation brutale ou destructive. Elle est réalisée par la combustion du réactif. A la suite de cette réaction, les liaisons de la chaîne carbonée de la molécule sont rompues. L’oxydation brutale par combustion est source d’énergie. L’éthanol est par exemple un composé chimique qui rentre dans la constitution des biocarburants. Au contraire, l’oxydation ménagée n’est pas fortement exothermique. L’oxydation ménagée peut être réalisée par exemple avec du permanganate de potassium. On appelle “oxydant” ce composé permettant la réaction d’oxydation. L’oxydation ménagée fait apparaître selon les conditions, divers produits de réaction :
- des aldéhydes
- des cétones
- des acides carboxyliques
Pour un alcool primaire
L’oxydation d’un alcool primaire conduit à la formation d’un aldéhyde et si l’oxydation se poursuit il se forme un acide carboxylique.
Exemple:
L’oxydation du butan-1-ol forme du butanal puis de l’acide butanoïque lorsque le réactif, ici l’ion permanganate, est en excès.

D'une façon plus générale, un alcool primaire fait partie du couple d’oxydo-réduction : R—CH2—OH / R—CHO et l'ion permanganate fait partie du couple: MnO4– / Mn2+. Voici les équations associées : 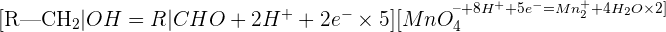
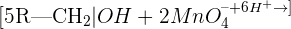
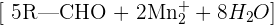 Un alcool primaire s’oxyde en aldéhyde. Il est donc le réducteur du couple oxydant / réducteur: aldéhyde / alcool primaire.
Un alcool primaire s’oxyde en aldéhyde. Il est donc le réducteur du couple oxydant / réducteur: aldéhyde / alcool primaire.
Si l’oxydant est en défaut :
Lorsque l’oxydation ménagée de l’alcool primaire est réalisée avec l’oxydant en défaut, il faut extraire l’aldéhyde formé du milieu réactionnel. En effet, la vitesse d’oxydation d’un aldéhyde étant plus grande que celle d’un alcool, en distillant l’aldéhyde, plus volatile que l’alcool primaire, on évite sa réaction d’oxydation en acide carboxylique.
Application de la vie courante :
Nous connaissons tous une application de l’oxydation de l’éthanol. C’est le test d’alcoolémie. L’oxydant est alors l’ion dichromate et il se transforme en ion chrome de coloration verte. L’intensité de la couleur permet de connaître la quantité d’éthanol présente au départ.
Pour un alcool secondaire
Cette oxydation ménagée conduit à une cétone. L’alcool secondaire est donc le réducteur du couple oxydant / réducteur : cétone / alcool secondaire. Une cétone est un composé organique comportant un groupe carbonyle. On reconnaît un groupe carbonyle grâce à sa double liaison entre une atome de carbone et un atome d’oxygène. Cette double liaison doit intervenir sur un carbone secondaire, c’est-à-dire lui-même lié à deux autres atomes de carbone. Une cétone peut être mise en évidence par sa réaction avec la DNPH et son absence de réaction avec le réactif de Schiff. Elle ne se poursuit pas jusqu'à un acide carboxylique même en présence d'un excès d'oxydant.
Exemple :
Avec l’équation d’oxydation du propan-2-ol par l’ion permanganate. Les couples sont MnO4 - /Mn2+ et C3H6O/C3H8O Les demi-équations sont : 
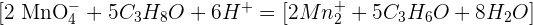
Application de la vie courante :
L’acide lactique est un des produits fabriqués par l’organisme lors de la production d’énergie par des muscles. Cet acide, bien connu des sportif est responsable de l’apparition des crampes lorsqu’il passe dans le sang lors d’un effort prolongé et d’une mauvaise oxygénation. C’est bien un acide : il contient à la fois une fonction acide carboxylique. C’est toutefois une molécule assez complexe car elle contient une fonction alcool secondaire. Lorsqu’il s’oxyde dans l’organisme, la réaction produit de l’acide pyruvique qui contient une fonction cétone.
Pour un alcool tertiaire
Les alcools tertiaires ne peuvent quant à eux pas être oxydés
Résumé
| alcool primaire | oxydation --> ménagée | Aldéhyde | oxydation --> ménagée | Acide carboxylique |
|---|---|---|---|---|
| alcool secondaire | oxydation --> ménagée | Cétone | oxydation --> ménagée | Rien |
| alcool tertiaire | oxydation --> ménagée | Rien |
Reconnaître les produits de l’oxydation ménagée d’un alcool
D’un point de vue expérimental, on utilise des réactifs pour identifier les composés chimiques produits par l’oxydation ménagée. Pour savoir si un alcool (primaire) a bien été oxydé en aldéhyde, il faut entreprendre le test à la D.N.P.H. La D.N.P.H. est l’abréviation de 2,4‑dinitrophénylhydrazine.
- Expérience :
Dans un tube à essai, introduire 1 mL de solution de D.N.P.H. et ajouter quelques gouttes du composé à tester.
- Résultat :
Si un précipité orangé se forme, c’est que nous sommes en présence d’un composé carbonylé (aldéhyde ou cétone). Pour caractériser un aldéhyde, le test à la D.N.P.H. ne suffit pas : il est nécessaire de compléter le protocole expérimental avec le test à la liqueur de Fehling.
- Expérience :
Verser dans un tube à essai, environ 2 mL de liqueur de Fehling et 1 mL du composé à tester. Chauffer doucement le mélange en agitant.
- Résultat :
Si un précipité rouge brique est formé, alors nous sommes en présence d’un aldéhyde. Si le composé testé a réagi au D.N.P.H. mais qu’il ne réagit pas à la liqueur de Fehling, alors sommes en présence d’une cétone.
Résumer avec l'IA :























Si vous désirez une aide personnalisée, contactez dès maintenant l’un de nos professeurs !
Très bien expliqué je me suis tout de suite retrouvé
Merci pour l’éclaircissement
Qu´elle est la source de l´alcool
Pourquoi n’ai je pas trouvé la formule générale des alcool ?
Bonjour, nous serions ravis de vous aider ! Avez-vous essayé de contacter l’un de nos professeurs pour recevoir une aide personnalisée ? Rendez-vous sur la plateforme de Superprof, sélectionnez la rubrique « Découvrir nos Superprofs » en indiquant la matière désirée. Vous trouverez de nombreux professeurs près de chez vous. Excellente journée ! :)
Chimie
je n’ai
pas trouver des exercices
Bonjour Elismé,
Les alcools sont présents dans de nombreux domaines de notre vie quotidienne. Le plus souvent, c’est l’alcool sous forme d’éthanol que nous rencontrons. Présent dans certains aliments, il est surtout présent dans les boissons alcoolisées. On le retrouve aussi dans les produits ménagers (notamment les produits de nettoyage de vitres, l’alcool permettant d’empêcher les traces sur les surfaces en verre).
Bonne journée