
Des molécules organiques carbonées
Les caractéristiques des alcanes
Les alcanes sont des molécules organiques uniquement composées d’atomes de carbone et d’hydrogène associés par des liaisons simples. Par cette association d’atomes de carbone et d’hydrogène, les alcanes sont aussi appelés “hydrocarbures” Comme toutes les molécules organiques l'enchaînement des atomes de carbone constitue le «squelette» de la molécule auquel sont liés les atomes d’hydrogène. La formule brute d’un alcane s’exprime ainsi : CnH2n+2 ou n est le nombre d’atomes de carbone.
Les caractéristiques des alcools
Les alcools ont une composition proche de celle des alcanes : ils sont également constitués d’atomes de carbone liés par liaison simples. La différence réside dans le fait que l’un des atomes d’hydrogène est remplacé par le groupe caractéristique hydroxyle (-O-H) Le groupe caractéristique hydroxyle est composé d’un atome d’oxygène et d’un atome d’hydrogène associés par une liaison simple. On exprime la formule brute d’un alcool de cette manière : CnH2n+1OH où n est le nombre d’atomes de carbone. Si plusieurs groupes caractéristiques hydroxyle (-OH) composent la molécule, on ne parle alors plus d’alcool mais de polyalcool.
Les règles de base pour nommer un alcane ou un alcool
Voici le principe de base pour nommer les composés organiques que sont les alcanes et les alcools : Le nom des alcanes est formé d’un terme dépendant du nombre d’atomes de carbone dans la chaîne, suivi du suffixe “ane”. Le nom des alcools est formé du même terme dépendant du nombre d’atomes de carbone de la molécule, suivi du suffixe “anol”.
| Nombre d’atome de Carbone | Formule brute | Préfixe | Alcanes : suffixe ANE | Alcools : suffixe ANOL |
|---|---|---|---|---|
| 1 | CH4 | méth | méthane | méthanol |
| 2 | C2H6 | éth | éthane | éthanol |
| 3 | C3H8 | prop | propane | propanol |
| 4 | C4H10 | but | butane | butanol |
| 5 | C5H12 | pent | pentane | pentanol |
| 6 | C6H14 | hex | hexane | hexanol |
| 7 | C7H16 | hept | heptane | heptanol |
| 8 | C8H18 | oct | octane | octanol |
| 9 | C9H20 | non | nonane | nonanol |
| 10 | C10H22 | déc | décane | décanol |
Les différentes structures des alcanes
Les alcanes sont des composés aliphatiques, par opposition aux composés aromatiques. On distingue trois catégories de chaînes carbonées. Ces trois catégories vont impliquer des règles particulières dans la définition de la nomenclature de ces composés organiques.
Les alcanes à chaîne linéaire
Chaque atome de carbone est lié à deux autres atomes de carbone par une liaison covalente simple. En fin de chaîne, l’atome de carbone est lié à 3 atomes d’hydrogène par des liaisons simples également. Exemple : Le propane : C3H8 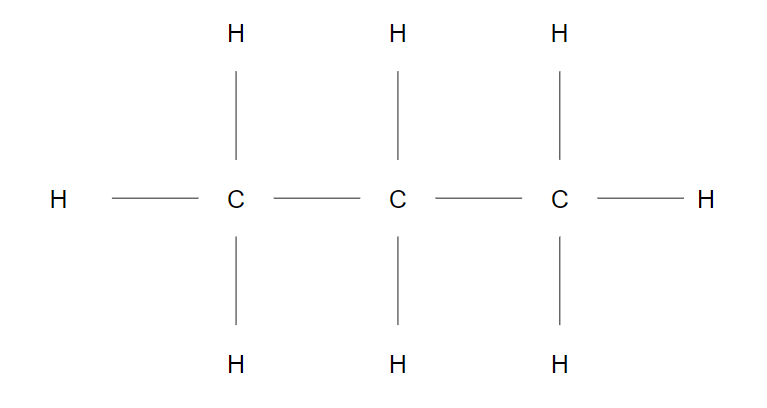
Les alcanes à chaîne ramifiée
On parle d’un alcane à chaîne ramifiée lorsqu’un atome d’hydrogène est remplacé par un groupement alkyle, c’est-à-dire un alcane auquel on aurait retiré son atome d’hydrogène terminal :
- CH3 : groupement méthyle,
- C2H5 : groupement éthyle,
- C3H7 : groupement propyle,
- C4H9 : groupement butyle
- etc.
Exemple : le groupement éthyle C2H5 : 

- Il est nécessaire de suivre ces étapes dans l’ordre : D’abord, repérer la chaîne carbonée la plus longue : combien y a-t-il d’atomes de carbone au maximum qui se suivent ? => Dans notre exemple, nous avons au maximum 5 atomes de carbone successifs.
- Ensuite, il faut numéroter les atomes de carbone de la chaîne carbonée la plus longue. => Voir la numérotation sur l’image ci-dessus.
- Puis, nous devons repérer les positions des groupements alkyles. => sur l’image ci-dessus, nous avons un groupement méthyle (-CH3) lié au troisième atome de carbone de la chaîne carbonée la plus longue.
- Comme la plus longue chaîne carbonée contient 5 atomes de carbone, nous sommes en présence d’un pentane auquel s’ajoute un groupement méthyle en 3e position. On nomme donc cette molécule :
=> le 3-méthylpentane
Autres règles :
- Si plusieurs groupements alkyles sont ajoutés à la chaîne principale, on énumère les positions et les types de groupement alkyle séparés par des tirets et rangés par ordre alphabétique. Exemple : 3-éthyl-2-méthylhexane
- Si plusieurs groupements alkyles identiques composent la molécule, on sépare les différentes positions de ces groupements alkyles par des virgules et on ajoute le préfixe “bi” si l'on compte deux groupements alkyles identiques, “tri” pour trois groupements alkyles identiques ou “quadri” pour quatre groupements alkyles identiques même si ce cas est beaucoup plus rare. Exemple : 2,3-diméthylhexane
- Il est nécessaire d’avoir les numéros de position des groupements alkyles les plus petits possibles. Ainsi, suivant les cas, on doit commencer la numérotation de la chaîne principale par la gauche ou par la droite.
Dans notre exemple ci-dessus, le groupement méthyle est placé sur le troisième atome de carbone quelque soit le sens de numérotation, de la gauche vers la droite ou bien de la droite vers la gauche.
Les alcanes à chaîne cyclique
Le nom d'un alcane à chaîne monocyclique sans chaîne latérale se forme en accolant le préfixe "cyclo" au nom de l'alcane à chaîne linéaire non ramifié possédant le même nombre d'atomes de carbone.
Exemple : le cyclohexane est un alcane composé d’une chaîne de 6 atomes de carbone réunis en un cycle.
La formule brute d’un alcane monocyclique peut s’exprimer ainsi : CnH2n Il existe également des composés de type alcanes monocycliques plus complexes. Ils portent une ou plusieurs chaînes latérales supplémentaires. Le nom des alcanes à chaîne monocycliques portant une ou plusieurs chaînes latérales est formé à partir de celui de l’alcane à chaîne monocyclique sans chaîne latérale correspondant et en indiquant la substitution selon les règles énoncées précédemment.
La numérotation le long du cycle est choisie de telle façon que l'atome de carbone portant le premier substituant par ordre alphabétique porte le numéro 1 et que le carbone portant le second substituant par ordre alphabétique porte le numéro le plus petit possible.
Exemple : le 1,2-diméthylcyclohexane, le 1-éthyl-3-méthylcyclopentane
Les règles de base pour nommer un alcool
Pour nommer un alcool, il est nécessaire de préciser la position du groupe caractéristique hydroxyle dans la chaîne carbonée. Comme pour les alcanes, il faut rechercher la chaîne carbonée la plus longue, c’est-à-dire celle comptant le plus d’atomes de carbones. Le nombre d’atomes de carbone ainsi trouvé donne le préfixe. On coupe ensuite le suffixe “anol” en deux parties séparées par la position du groupe caractéristique -OH :
préfixe + “an” + -position- + ”ol”
Exemple : Ici, nous avons 5 atomes de carbone (en noir) et le groupe caractéristique hydroxyle (en rouge) positionné sur le troisième atome de carbone. Lorsque 5 atomes de carbone composent la chaîne principale, on utilise le préfixe “pent”. En suivant la règle citée ci-dessus, nous obtenons : le pentan-3-ol 
Les différentes classes d’alcools
Les alcools sont classés en trois classes :
- primaire,
- secondaire
- et tertiaire.
Pour déterminer à quelle classe un alcool appartient, il convient de repérer le nombre de radicaux organiques liés à l’atome de carbone portant le groupe caractéristique hydroxyle (-OH).
Les alcools primaires
Un alcool primaire se reconnaît par la présence d’un seul radical organique (bien souvent le groupement alkyle) sur l’atome de carbone possédant le groupe caractéristique hydroxyle. On les note ainsi :
R-CH2-OH où R est le radical organique
Exemple :
l’éthanol = CH3-CH2-OH
Les alcools secondaires
Un alcool secondaire se reconnaît par la présence de deux radicaux organiques (R et R’) sur l’atome de carbone possédant le groupe caractéristique hydroxyle. Exemple : le propan-2-ol 
Les alcools tertiaires
Un alcool tertiaire se reconnaît par la présence de trois radicaux organiques (R, R’ et R’’) sur l’atome de carbone possédant le groupe caractéristique hydroxyle. Exemple : le 2-méthylpropan-2-ol 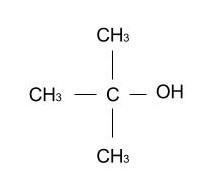
Exemple avec l’isomérie de position
Des isomères sont des molécules qui ont à la fois une configuration atomique différente et une formule brute identique. Dans l’exemple suivant, nous comparons trois molécules dont la formule brute est semblable : C4H10O. Nous parlons d’isomérie de position car dans chacun des cas, la position du groupe caractéristique hydroxyle est différente.
Cas du butan-1-ol

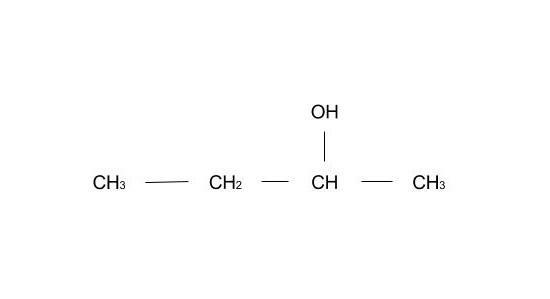
Cas du butan-2-ol
Cas du 2-méthylpropan-2-ol

Résumer avec l'IA :























Si vous désirez une aide personnalisée, contactez dès maintenant l’un de nos professeurs !
J’ai aimé vos explications.
modiat de sa
Bonsoir ! J’ai une question sur les alcools , s’il vous plaît !
Besoins d’aide en chimie,cool votre procédure pour aider le monde
Bonjour, merci pour votre retour. Il nous ferait plaisir de vous aider, n’hésitez pas à contacter nos professeurs sur la plateforme de Superprof :)
C’est trop cool
Merci beaucoup. Ce cours est très précis.
C’est vraiment très précis merci beaucoup.! 5/5
Merci beaucoup pour votre aide