
I/ Interactions fondamentales:
A) Particules élémentaires
Définition:
On appelle particule élémentaire toute particule indivisible (cette notion est évidemment liée à l'état des connaissances actuelles).
|
| Caractéristiques des particules élémentaires dans l'atome | |||
| Proton | mp = 1,67.10-27kg | q = +e | r = 1,2.10-15m |
| Neutron | mn = 1,67.10-27kg | q = 0 | r = 1,2.10-15m |
| Électron | me = 9,11.10-31kg | q = -e | |
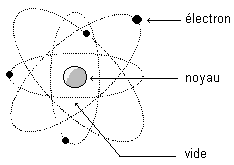
B) Les interactions fondamentales
La cohésion de la matière est due aux interactions entre les particules élémentaires:
- L'interaction gravitationnelle (Newton 1867) entre les masses.
- L'interaction électrique (Coulomb 1785) entre les charges.
- L'interaction forte (1970) entre les nucléons.
II/ Cohésion de la matière
A) A l'échelle du noyau atomique
Rappel: Interaction gravitationnelle: (voir cours de seconde).Deux corps A et B de masses respectives mA et mB séparés d'une distance d exercent l'un sur l'autre des forces opposées 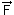
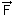
| avec G = 6,67.10-11 N.m2.kg-2 |
Soit un noyau d'hélium 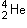
Interaction gravitationnelle: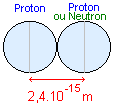
| => |
| ||||||||||
| => | Fp/p = 3,23.10-35N |
Interaction électrique: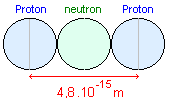
| => |
| ||||||||||
| => | Fp/p = 10N |
La force de répulsion électrique est très supérieure à la force d'attraction gravitationnelle. La cohésion des noyaux ne peut être due aux deux forces précédentes (les noyaux se disloqueraient).
La cohésion des noyaux est donc due à l'interaction forte.
Définition: L'interaction forte est une interaction attractive importante qui s'exerce sur les nucléons. Elle assure la cohésion des noyaux.
Remarque: Contrairement à l'interaction gravitationnelle et à l'interaction électrique, l'interaction forte augmente avec la distance. Cependant, c'est une action à courte portée.
B) A l'échelle atomique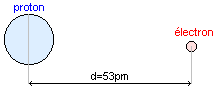

Soit un atome d'hydrogène 
Déterminons la valeur des interactions gravitationnelles et électriques qui existent entre le noyau et l'électron de cet atome.
Interaction gravitationnelle:
| => |
| ||||||||||
| => | Fp/e = 3,61.10-47N |
Interaction électrique:
| => |
| ||||||||||
| => | Fp/p = 8,20.10-8N |
La force d'attraction électrique est très supérieure à la force d'attraction gravitationnelle. L'interaction électrique assure la cohésion de la matière à l'échelle atomique.
C) A l'échelle moléculaire et à notre échelle
Un calcul identique au niveau de la molécule donne le même résultat. Les propriétés des solides, des liquides et des gaz en découlent. La cohésion de la matière à l'échelle moléculaire est assurée par l'interaction électrique.
D) A l'échelle astronomique
A l'échelle de l'Univers, la matière est électriquement neutre. Seule l'interaction gravitationnelle assure la cohésion de la matière à l'échelle de l'Univers. Elle est responsable du mouvement des astres, de la formation des étoiles, des planètes et des galaxies.
Résumer avec l'IA :























Si vous désirez une aide personnalisée, contactez dès maintenant l’un de nos professeurs !
Bonjour j’aurais besoin d’avoir des cours de soutien actuellement en première avec spé maths et physique pour l’année suivante je souhaite m’améliorer encore plus et me préparer pour le bac
Bonjour Sandi, tu vas surement trouver le meilleur prof de soutien sur notre plateforme. :)