Chapitres

Présentation du platine
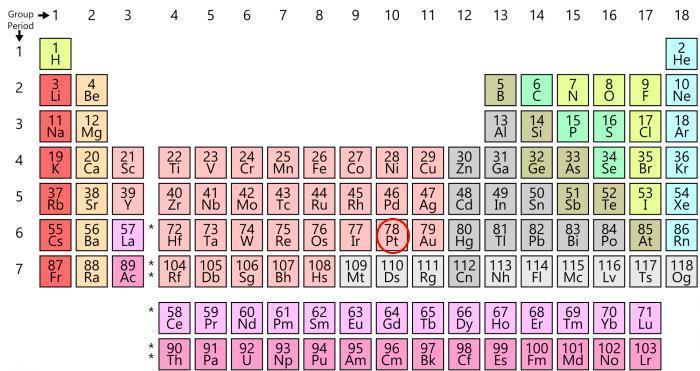
| Informations générales | |
|---|---|
| Symbole | Pt |
| Numéro atomique | 78 |
| Famille | métaux de transitions |
| Groupe (colonne) | 10 |
| Période (ligne) | 6 |
| Bloc (sous couche électronique) | d |
| Propriétés atomiques | |
| Masse atomique (isotope principal) | 195 u |
| Structure électronique | (K)2(L)8(M)18(N)30(O)17(P)1 |
| Configuration électronique | 1s22s22p63s23p63d104s24p64d104f145s25p65d96s1 |
| Propriétés physico-chimique | |
| électronégativité | 2,28 |
| Masse molaire atomique (g/mol) | 195,1 |
Il est considéré comme plus précieux que l'or, c'est pourquoi un disque de platine est supérieur à un disque d'or et qu'il faut 70 ans de mariage pour fêter ses noces de platines contre "seulement" 50 pour celle d'or.
C'est un métal très peu réactifs, ce qui lui permet d'avoir une forte résistance à la corrosion et à l'oxydation, à part dans des conditions de fortes températures. Il est cependant le plus réactif de ses homologues platinoïdes. Par ailleurs, ils a d'importantes capacités à catalyser les réactions chimiques (c'est-à-dire accélération de la réaction chimique, ou amélioration de son rendement, afin de la rendre rentable). Au niveau de ses propriétés mécaniques, le platine a un comportement plus proche de l'or que les autres platinoïdes, car c'est un métal mou et ductile.
Origine - étymologie
"Platine" provient de l'espagnol "platina" qui signifie "petit argent". Ce terme a été choisi lors de sa découverte en Amérique du sud où il était d'abord considéré comme une impureté de l'argent.
La découverte du platine, un peu d'histoire
Le platine est connu depuis l'époque précolombienne en Amérique du sud où il était utilisé sous forme pure ou d'alliages, pour réaliser de petits objets ou des bijoux. Cependant, les européens ne le découvrent qu'avec leur arrivée sur le nouveau continent.
La première mention de ce métal est faite en 1557 par l'italien Julius Caesar Scaliger qui le décrit comme un métal mystérieux provenant de mines d'Amérique centrale, que les techniques espagnoles de l'époque ne permettent pas de fondre.
En 1741, le scientifique et métallurgiste britannique Charles Wood ramène des grains de platine de Jamaïque en espérant leur trouver une application. Quelques années plus tard, en 1748, l'astronome Antonio de Ulloa publie le compte rendu d'une étude sur le platine réalisée lors d'une expédition scientifique de près de 10 ans en Amérique du sud. Le chimiste William Brownrigg et le physicien William Watson les étudient et présentent en 1750 les résultats de leurs recherches. Ils sont les premières à considérer le platine comme un métal à part entière.
Les Origines du platine sur Terre
L'origine du platine (ainsi que des métaux platinoïdes) sur Terre serait d'origine extra-terrestre, ce qui expliquerait sa présence à la surface de la terre alors que c'est un métal sidérophile (présentant une forte affinité avec le fer) et devrait donc se situer proche du noyau terrestre. Des chercheurs australiens étudiant la composition de laves anciennes, les komatites, pensent en détenir la preuve. Ces laves sont issues d'activités volcaniques ayant eu lieu à la fin du temps géologique nommée archéen (- 4000 millions d'années). Ces chercheurs se sont aperçus que la teneur en platine augmente au sein de ses laves suivant leur "âge" : plus elles sont récentes plus le platine y est présent. Ceci va dans le sens d'une arrivée tardive du platine à la surface de la terre.
Les principaux isotopes du platine
Isotopes non radioactifs
Le platine possède cinq isotopes naturels allant de l'isotope 192 à l'isotope 198. Les isotopes 195 et 194 sont les plus abondants, présents quasiment à des proportions identiques, respectivement 33,8 % et 32,9 %. L'isotope 196 est également très présent car représente en proportion un quart de ces isotopes naturels. Les isotopes 198 et 192 sont nettement moins abondants, car moins stables, avec respectivement des proportions de 7,2 % et 0,79 %.
Radioisotopes naturels
Il existe un seul et unique radioisotope du platine naturel. Celui-ci a un nombre de masse de 190 et est très peu présent sur terre (0,01 %). Ce radioisotope demeure relativement stable avec une période de demi-vie de 650 milliards d'années et se désintègre selon un processus α.
Isotopes synthétiques
Il existe de nombreux isotopes synthétiques du platine obtenus dans les laboratoires de recherche en radiochimie. Les isotopes plus légers que le platine naturels ont des nombres de masses allant de 166 à 189. Chacun de ces isotopes a deux modes de désintégration possibles : α ou β+. Plus l'isotope est léger plus la désintégration α prédomine, par contre plus l'on se rapproche des isotopes naturels plus la désintégration β+ s'accentue puis prédomine. Les isotopes plus lourds que les isotopes naturels du platine sont nettement moins nombreux et ont des nombres de masses de 199 à 202. Ces isotopes se désintègrent principalement selon une radioactivité β-.
Le platine sous forme de corps simple
C'est un métal gris clair brillant, malléable, ductile, qui ne réagit pas avec le dioxygène, ni l'eau ou la plupart des acides. Cependant, il réagit à l'eau régale (mélange d'acide chlorhydrique et nitrique concentrés). Il globalement presque chimiquement inerte mais à haute température il peut cependant réagir avec les bases. Il réagit également avec les dihalogènes. Il présente la particularité d'absorber jusqu'à 743 fois son propre volume en dihydrogène. En effet, un atome de platine est capable de se lier à un atome d'hydrogène de manière non covalente : c'est une liaison appelée liaison métallique. Ceci est dû à la présence d'électrons non appariés à la surface de l'atome de platine et aux propriétés d'accepteurs d'électrons de l'ion hydrogène. C'est de cette propriété que découle de nombreuses applications.
Les ions du platine en solution aqueuse
Le platine forme un ion en solution aqueuse de formule Pt-4+ : c'est un cation monoatomique qui présente un défaut de 4 électrons.
Composés à base de platine
Nous l'avons vu le platine réagit avec les halogènes. Un exemple est l'hexafluorure de platine de formule PtF6 : c'est solide rouge fortement oxydant qui peut être obtenu par réaction chimique entre le platine métallique et le difluor. Avec le fluor, il peut également formé le PtF4 et PtF5. De la même manière il réagit avec le chlore et le brome pour former :
- PtCl2, PtCl3
- PtBr2, PtBr3
Le platine a également la propriété de former des complexes moléculaires.
La production terrestre de platine

Les utilisations du platine
Les utilisations du platines sont variées. Ces propriétés mécaniques et esthétiques en font le métal le plus précieux pour la bijouterie. Ces propriétés de conduction électrique et catalytique en font également un métal de choix pour l'industrie de l’électronique, automobile et de la chimie. Ses propriétés mécaniques, ainsi que son interaction avec certains systèmes vivants, lui confère également un intérêt médical.
Les applications industrielles
Le platine peut être utilisé, à l'image d'autres métaux platinoïdes et de l'or dans les contacts électriques extrêmement durables dans le temps. Grâce à ses propriétés de catalyseurs de réaction chimiques il peut être utilisé pour les pots catalytique (accélérateurs de décomposition des gaz nocifs), bien qu'il soit de plus en plus remplacé par du palladium, moins onéreux. Du fait de sa capacité à capter l'hydrogène en grande quantité, qu'il relargue après chauffage, cet élément est à l'étude pour une utilisation dans les piles à combustible.
Son utilisation en chimie
Le platine étant un excellent catalyseur, il est très souvent utilisé dans l'industrie chimique sous forme de filet métallique afin de permettre l'exploitation de certaines réactions chimiques :
- Production d'acide nitrique à partir d’ammoniac.
- Raffinage du pétrole.
- Production de formaldéhydes à partir de méthanol pour les briquets notamment.
Les applications médicales
Le platine est utilisé pour ses propriétés mécaniques en alliage avec osmium (90/10) en chirurgie cardiaque. Il intervient également au sein de complexes moléculaires efficaces contre certains cancers (leucémie, testicule, vessie). En effet ces complexes contenant du platine, ont la capacité de détruire l'ADN des cellules cancéreuses en créant des liaisons covalentes sur un des brins d'ADN, entraînant sa déformation et donc la mort de la cellule. Malheureusement, ces complexes, très réactifs, entraînent de lourds effets secondaires.
La bijouterie
Le platine est considéré comme le métal le plus précieux en bijouterie. Naturellement blanc, il se compare à l'or blanc. Il est plus cher que l'or blanc notamment car il contient 95 % de platine (platine 950) contre 75 % d'or dans l'or blanc. De plus, le platine, plus rare que l'or, est également plus cher à l'origine. Le platine a de nombreux avantage par rapport à l'or blanc :
- Il permet une meilleure tenue des pierres précieuses.
- L'or blanc peut légèrement jaunir avec le temps.
- Il ne provoque aucune allergie contrairement à l'or.
Par contre, il est plus mou que l'or et est donc plus sensible aux rayures et pourra se déformer un peu plus facilement. Enfin, le platine est légèrement plus dense que l'or, le bijou sera donc un peu plus lourd pour des dimensions identiques. 
Sources : - "Chemical elements how they were discovered" - D.N. et V.D. Trifonov p 82 à 84 - "Chemical elements 2nd edition" - David E Newton p 431 à 436
Résumer avec l'IA :























Si vous désirez une aide personnalisée, contactez dès maintenant l’un de nos professeurs !