
Carte d'identité du Magnésium
Le Magnésium est un élément chimique métallique, de symbole atomique Mg et de numéro atomique Z = 12. Sa structure électronique est donc la suivante : (K)2(L)8(M)2 soit 12 électrons répartis dans les différentes couches. Dans le tableau périodique, il est situé sur la troisième période et dans la deuxième colonne : il appartient à la famille des alcalino-terreux. 
| Symbole atomique: Mg Numéro atomique: Z= 12 Principal isotope: A= 24 Structure électronique: (K)2(L)8(M)2 Couche externe: M Répartition des électrons externes: deux électrons non appariés Nombre de liaisons formées dans une molécule: 2 Configuration électronique: 1s22s22p63s2 Période: 3 Groupe: 2 Famille: métaux alcalino-terreux Electronégativité: 1,31 Masse molaire atomique: 24,3 g/mol | Représentation de Lewis 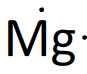 Localisation dans la classification Localisation dans la classification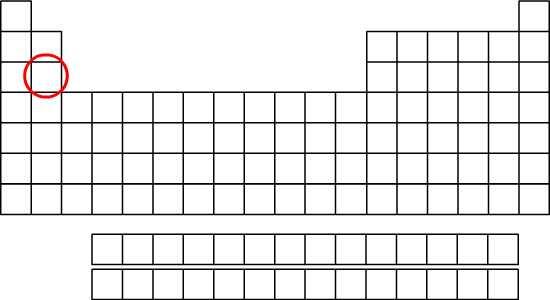 |
Histoire du Magnésium
Origine du mot Magnésium
Le mot Magnésium a été formé à partir du mot "Magnesia", qui est le nom d'un district de Thessalie, très riche en Magnésium sous différentes formes, et notamment en Carbonate de Magnésium. Initialement, le scientifique étant le premier à avoir réussi à isoler du Magnésium pur, Humphry Davy, avait proposé le nom "Magnium".
La découverte du Magnésium : un peu d'histoire
En 1755, le chimiste écossais Joseph Black reconnut le Magnésium comme un élément chimique. Ce n'est qu'en 1808 que le chimiste britannique Humphry Davy est parvenu à obtenir du Magnésium métallique par électrolyse d'un mélange de Magnésite (MgCO3) et d'Oxyde de Mercure (HgO) fondu. Cependant, il n'est pas parvenu à le purifier totalement. Finalement, en 1831, le chimiste français Antoine Alexandre Brutus Bussy a réussi à mettre au point une méthode qui permet d'obtenir du Magnésium pur.
Les principaux isotopes du Magnésium
Le Magnésium possède 22 isotopes connus.
Isotopes du Magnésium présents dans la nature
Parmi les 22 isotopes du Magnésium, trois d'entre eux sont stables et présents dans la nature :
- l'isotope de nombre de masse A = 24, celui-ci étant le plus abondant, présent à 79% par rapport aux deux autres
- l'isotope de nombre de masse A = 25, représentant 10% du Magnésium naturellement présent
- l'isotope de nombre de masse A = 26, représentant également 11% du Magnésium présent dans la nature
Le tableau ci-dessous résume ces informations.
| Z = 12 - A = 24 | Z = 12 - A = 25 | Z = 12 - A = 26 | |
| Symbole du noyau | 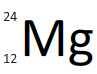 | 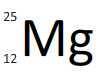 | 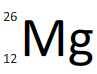 |
| Composition du noyau | 12 protons 12 neutrons | 12 protons 13 neutrons | 12 protons 14 neutrons |
| Proportion sur Terre | 78,99 % | 10 % | 11,01 % |
Isotopes radioactifs du magnésium
Les 19 autres isotopes du Magnésium sont donc radioactifs : ce sont des radioisotopes. L'isotope de nombre de masse A = 28 est celui qui a le temps de demi vie le plus long, autour de vingt heures. Le Magnésium 27 a lui une durée de demi vie environ égale à neuf heures. Tous les autres radioisotopes ont des temps de demi vie inférieurs à la minute, voire même inférieurs à la seconde.
Le Magnésium sous ses différentes formes
Le Magnésium sous forme de corps simple
Généralités à propos du Magnésium sous forme de corps simple
Le Magnésium est le huitième élément le plus abondant de la couche terrestre, et le neuvième dans l'Univers. Sous forme atomique, il se présente sous la forme d'un métal grisâtre, peu dense, facilement inflammable qui brûle en émettant une lueur blanche intense.
Réactivité du Magnésium sous forme de corps simple
La réaction du Magnésium avec l'eau n'est possible qu'à chaud et elle produit alors de l'oxyde de Magnésium (MgO) et du Dihydrogène (H2) suivant l'équation de réaction chimique suivante :
Mg + H2O -> MgO + H2
Le Magnésium peut également réagir avec le Dioxygène (O2) de l'air pour donner de l'Oxyde de magnésium (MgO) :
- soit à froid : l'Oxyde de magnésium constitue alors une couche qui ternit le métal et le protège d'une oxydation en profondeur
- soit à chaud : lors d'une combustion
L'équation de la réaction de transformation chimique est alors la suivante :
2Mg + O2 -> MgO
La combustion du magnésium dans l'air inclus également une réaction avec le diazote qui conduit à la formation de nitrure de magnésium suivant la réaction de transformation chimique suivante :
3Mg + N2 -> Mg3N2
Enfin, le Magnésium peut aussi réagir avec certains dihalogènes comme par exemple le Brome ou encore le Chlore pour former des halogénures de magnésium, suivant les réactions de transformation chimique suivantes :
2Mg + Cl2 -> 2MgCl
2Mg + Br2 -> 2MgBr
Les ions Magnésium
En solution aqueuse, le Magnésium se présente sous forme d'ion de formule Mg2+. Il s'agit d'un cation possédant deux électrons de moins que l'atome de Magnésium. On le retrouve fréquemment associé à divers anions de minéraux. En effet, il peut former facilement des sels solubles dans l'eau, tel que le Chlorure de Magnésium. A noter que sous forme ionique il joue un rôle biologique essentiel aussi bien chez les plantes que les animaux.
Corps composés à base Magnésium

Le rôle biologique du Magnésium
Le Magnésium joue un rôle essentiel dans le bon fonctionnement du corps humain. La liste peut être très longue, mais on peut tout de même citer son intervention dans :
- la formation des os, des dents
- la fixation du Calcium
- la lutte contre le stress
- la transmission de l'influx nerveux
Il est donc important d'apporter aux corps les quantités indispensables en Magnésium afin de ne pas avoir des carences. Cela passe par une alimentation adaptée et équilibrée. Les céréales contiennent notamment du Magnésium.
Les applications du Magnésium
De part son abondance naturelle, le Magnésium intervient dans de nombreuses applications. Le Magnésium est beaucoup utilisé dans des applications où la réduction du poids est un objectif. En effet, sa légèreté fait de lui un métal de choix, car il est trois fois moins dense que l'Aluminium. Les applications sont donc nombreuses dans le domaine de l'aéronautique ou de l'automobile. 
- boîtiers d'ordinateurs portables,
- armatures des sièges,
- tableaux de bord dans les automobiles
- ou encore les TGV.
D'autres types d'alliages font intervenir le Zinc, ou encore le Zirconium. Enfin, c'est également un réactif important dans le secteur de l'industrie chimique, très utilisé dans les procédés désulfuration, au cours de la fabrication des aciers ou encore la purification des métaux.
Résumer avec l'IA :























Si vous désirez une aide personnalisée, contactez dès maintenant l’un de nos professeurs !
Super article.
Merci pour toutes ces informations. Vous indiquez que le magnésium ne réagit pas dans l’eau froide. (pas d’oxydation)
J’utilise du magnésium sous forme de bille pour remplacer la lessive. À froid j’observe une augmentation significative du pH de l’eau. Les billes étant ensemble dans un sachet, le magnésium s’oxyde à l’air. Une fois dans la machine cet oxyde se détache suite à l’effet d’abrasion produit par le frottement des billes les unes contre les autres. Pouvez-vous m’expliquer la réaction chimique qui intervient dans ce cadre-là ?
Bonjour, merci pour votre retour ! Il nous ferait plaisir de vous aider, n’hésitez pas à contacter nos professeurs sur la plateforme de Superprof. Bonne journée ! :)