
Introduction
Un petit rappel sur les réactions de combustion qui posent parfois des problèmes (surtout au niveau de l'équilibrage des réactions) Une réaction de combustion classique (du moins au niveau collège/lycée) consiste à "brûler" un composé organique (de formule générale CxHyOz) par de l'oxygène pour donner, dans le cas d'une combustion complète (ce qui est le cas dans tous les énoncés d'exercices sauf indication contraire), uniquement de l'eau H2O et du dioxyde de carbone CO2.

Le carbone
Histoire et découverte
Dès l'Antiquité, les Romains ont commencé à fabriquer du carbone avec du charbon de bois par des techniques de carbonisation du bois sous terre. Dans l'Asie Antique, le carbone était déjà présent sous forme de diamants. Il faut cependant attendre le XVIIIe siècle pour que les chimistes se penchent de plus près sur le cas du carbone. C'est Antoine Lavoisier en 1772 qui va commencer à étudier la combustion des diamants et du charbon, deux composés qui proviennent uniquement du carbone. Il remarquera notamment que lors d'une combustion de carbone, il n'y a pas de formation d'eau contrairement aux autres combustions.
Antoine Laurent Lavoisier était un chimiste philosophe et économiste français du XVIIIe siècle. Il est reconnu pour la mise en place de nombreuses méthodes scientifiques que ce soit dans le domaine des expériences ou de la théorie. Il a notamment découvert les composantes de l’air et de l’eau, les différents états de la matière et a défini ce qu’était l’oxydation. Il est considéré comme le père de la chimie moderne On lui doit la célèbre maxime "Rien ne se perd, rien ne se crée, tout se transforme"
En 1828, Friedrich Wöhler, un chimiste allemand, découvre la chimie organique dans laquelle le carbone a un rôle primordial. La dernière découverte notable impliquant le carbone est la découverte du graphène par André Geim, un physicien néerlandais, en 2004.
La présence du carbone sur Terre

Le carbone est principalement présent à l'état naturel sous deux formes allotropiques : le graphite et le diamant.
L'allotropie est la faculté de certains corps simples d'exister sous plusieurs formes cristallines ou moléculaires différentes. Une forme allotropique peuvent avoir des propriétés physique, comme la couleur et la dureté, et une réactivité chimique différentes même si elles sont composées d'atomes identique Les transformations d'une forme allotropique à l'autre peuvent être induites par des changements de pression et de température ou même par une réaction chimique. Certaines formes ne sont stables que sous certaines conditions définies de température et de pression
A pression et température ambiantes, le carbone se trouve sous sa forme de graphie à l'état naturel. Il est apparu sur Terre dès la création de cette dernière comme en témoigne sa présence dans de nombreux sédiments (pétrole par exemple). On peut pour finir le trouver sous d'autres formes comme :
- Charbon,
- Pétrole,
- Sédiments.
Le dioxyde de carbone, de formule , est présent quant à lui dans l'atmosphère sous forme de gaz et dans les eaux océaniques et continentales, sous forme de gaz dissout.
Les propriétés chimiques du carbone
Le carbone est un élément non soluble dans l'eau ainsi que dans aucun solvant organique. Quand il est fortement chauffé, il s'oxyde pour former du monoxyde de carbone et du dioxyde de carbone. Lié à l'hydrogène, le carbone est source de vie. Cette liaison apparaît dans chaque être vivant organique de la planète. Le carbone compte 15 isotopes connus à ce jour. Leur nombre de masse s'étend de 8 à 22. Le radioisotope le plus stable est la carbone 14, présent à l'état naturel avec une demi-vie d'environ 5000 ans.
Des isotopes sont des atomes qui possèdent le même nombre de protons mais un nombre différent de neutrons
L'oxygène
Du fait de la configuration électronique de ses électrons de valence, l'oxygène a six électrons disponibles. Quatre électrons forment deux doublets non liants. Il reste donc deux électrons très disponibles pour réagir avec d'autres éléments chimiques, c'est pourquoi l'oxygène peut se lier à la plupart des autres éléments chimiques. Ainsi, on ne retrouve pas l'élément oxygène à l'état natif sur terre. Cependant, nous sommes entourés de dioxygène, c'est pourquoi la confusion est fréquente entre oxygène et dioxygène. Les principaux corps simples formés de d'oxygène sur terre sont :
- Le dioxygène, de formule O2, est une molécule composée de deux atomes d'oxygène. Il s'agit d'un des deux gaz majoritaires constituant l'air (environ 21%). Il permet la respiration animale, intervient dans les combustions, provoque l'oxydation de la plupart des métaux mais ne réagit pas avec l'eau ni les autre constituants de l'air.
- L'ozone de formule O3 est une molécule composée de trois atomes d'oxygène, c'est un oxydant encore plus puissant que le dioxygène. Il est donc très réactif. Au niveau du sol, c'est un polluant nocif, irritant pour les poumons, mais la couche qu'il forme dans la stratosphère (entre 20 et 50 km d'altitude) nous protège des rayonnements ultraviolets les plus nocifs. Ce que l'on appelle communément le "trou" dans la couche d'ozone, est plus précisément un amincissement de cette couche, accentué par l'activité humaine. En effet certains gaz contenant du chlore ou du brome (très utilisés dans les réfrigérateurs dans les années 70-80), relargués dans l'atmosphère se dissocient sous l'effet des rayons solaires (UV), et libèrent du chlore et du brome. Ces éléments sont des catalyseurs de la dégradation de l'ozone.

Équilibrer une équation
Reste maintenant à équilibrer l'équation (c'est à dire à trouver les coefficients stoechiométriques des réactifs et des produits). On cherche ainsi à écrire que ce qui est à gauche de la flèche de réaction est égal à ce qui est à droite (principe de conservation de la matière). Dans l'ordre, on équilibre d'abord les atomes de carbone, puis les atomes d'hydrogène et enfin les atomes d'oxygène (cette méthodologie est générale pour équilibrer n'importe quelle réaction et elle évite les erreurs lors de réactions plus compliquées à équilibrer) Essayez de faire attention à ne pas tourner en rond lorsque vous mettez des indices et veillez aussi à ce que ces indices soit les plus petits entiers possibles! Un petit exemple pour illustrer mes propos:
Ecrire l'équation de combustion du propane
Le propane à pour formule brute C3H8. L'équation de combustion s'écrit donc 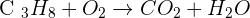
Équilibrons maintenant la réaction
- 3 atomes de carbone à gauche et 1 à droite. Il faut donc multiplier par 3 le terme C02 à droite:
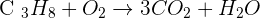
- 8 atomes d'hydrogène à gauche et 2 à droite. Il faut donc multiplier par 4 le terme H2O à droite:
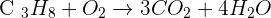
- 2 atomes d'oxygène à gauche et 3*2 + 4*1=10 à droite. Il faut donc multiplier par 5 le terme O2 à gauche:

- Les coefficients trouvés sont les plus petits entiers possibles.
L'équation de la réaction de combustion est donc:  Voilà, maintenant plus de raison de se tromper dans les réactions de combustion !!
Voilà, maintenant plus de raison de se tromper dans les réactions de combustion !!
Les dangers : émission de gaz toxique
Tous les ans, en hiver, des dizaines de personnes s'intoxiquent en utilisant un appareil de chauffage. Quel est le gaz responsable de cette intoxication ? Comment est-il produit ? Réponse : lors d'une combustion incomplète, un gaz très toxique, le monoxyde de carbone, est produit. Dans quelles conditions ce gaz est-il produit ? Quels sont les autres dangers des combustions domestiques ?
Le monoxyde de carbone : l'ennemi inodore et incolore
La combustion des hydrocarbures produit du dioxyde de carbone. Quand le dioxygène est en quantité suffisante, la combustion est complète mais s'il n'y a pas assez de dioxygène, la combustion est incomplète et du monoxyde de carbone est produit. C'est un gaz incolore, inodore et toxique. Il empêche le dioxygène de circuler dans le sang et provoque l'asphyxie de l'organisme qui peut conduire à la mort. Les symptômes d'une intoxication peuvent être un endormissement et des nausées. Le monoxyde de carbone est l'un des oxydes du carbone. De formule CO, il se compose d'un atome de carbone et d'un atome d'oxygène. A température ambiante et dans des conditions normales de température, le monoxyde de carbone est incolore et inodore. Il est donc impossible de sentir sa présence pour un homme.
Les intoxications au monoxyde de carbone
Ces intoxications ont souvent lieu l'hiver. Elles sont dues à un mauvais fonctionnement des appareils de chauffage ou à une mauvaise aération. En effet, si un local est trop hermétiquement fermé pour éviter que l'air froid ne rentre, le dioxygène consommé par les combustions n'est pas remplacé. On s'expose alors à deux risques : La quantité de dioxygène dans l'air étant trop faible, les poumons ne peuvent oxygéner suffisamment le sang et donc le cerveau. Ceci peut entraîner une perte de connaissance, voire la mort. La quantité de monoxyde de carbone dans l'air augmente, entraînant une intoxication rapide. Pour supprimer ces deux risques, il faut donc aérer les lieux où sont réalisées des combustions et faire vérifier régulièrement les appareils fonctionnant au gaz.
Les explosions provoquées par le monoxyde de carbone
Dans un brûleur de cuisinière fonctionnant au gaz, la réaction de combustion est contrôlée car le butane et le dioxygène de l'air réagissent au fur et à mesure qu'ils se mélangent. La combustion consomme de petites quantités de réactifs. Les explosions arrivent quand de grandes quantités de réactifs sont mélangées, à la suite d'une fuite de gaz par exemple. Au contact d'une source de chaleur comme une étincelle, la réaction de combustion démarre et dégage instantanément beaucoup de chaleur, tous les gaz présents se dilatent en produisant le bruit et le souffle de l'explosion.
Les appareils susceptibles de créer du monoxyde de carbone
Tous les appareils dans lesquels se produisent une combustion incomplète peuvent produire du monoxyde de carbone. Cette réaction peut avoir lieu quel que soit le combustible. Cela peut être :
- Du pétrole ;
- Du bois ;
- De l'essence ;
- Du fioul ;
- Du gaz (butane, propane ou autre) ;
- Du charbon ;
- Du gasoil.
Le dégagement de monoxyde de carbone peut avoir lieu pour plusieurs raisons. Il peut s'agir de l'évacuation des fumées qui est mauvaise et donc ces dernières refoulent dans la pièce et se retrouvent dans l'air respiré ou alors il peut s'agir d'un manque d'entretient des appareils de chauffage. En effet, ces derniers s'ils ne sont pas régulièrement entretenus peuvent ne pas laisser passer les bonnes quantités d'air ou de combustible et donc causer des combustions incomplètes, génératrices de monoxyde de carbone. Pour finir, le non respect des conditions d'utilisation des appareils peut être la cause d'une intoxication au monoxyde de carbone. Il ne faut jamais utiliser un appareil destiné à chauffer à l'extérieur (chauffage au fioul par exemple) dans un espace confiné ou à l'intérieur. Ces derniers ont été conçus pour fonctionner avec la ventilation naturelle de l'air extérieur. Une fois privé de ce dernier, ils peuvent alors fumer et causer des vapeurs nocives.
Les symptômes de l'intoxication et comment s'en protéger

Lorsque l'on est victime d'une intoxication au monoxyde de carbone, on peut ressentir certains symptômes. Cependant, c'est qu'il est déjà trop tard et que le gaz toxique a déjà pénétré dans notre organisme. Voici les symptômes que l'on peut être amenés à ressentir lors d'une intoxication au monoxyde de carbone :
- Maux de tête ;
- Propos incohérents ;
- Fatigue soudaine ;
- Nausées ;
- Vertiges ;
- Malaises ;
- Asthénie.
Dans les cas d'intoxication les plus graves, la personne peut aller jusqu'à se retrouver dans le coma et décéder. Afin de se protéger des intoxications au monoxyde de carbone, divers solutions existent. On peut par exemple s'équiper d'un détecteur de monoxyde de carbone. Ce dernier vous avertira de la présence de monoxyde de carbone dans l'air, comme le ferait un détecteur de fumée avec un départ de feu. Des bonnes pratiques existent aussi concernant vos appareils de chauffage. Faites les réviser régulièrement et effectuez des ramonages des conduits d'évacuation des fumées. De plus, même en plein hiver, aérez bien les espaces dans lesquels fonctionnent des appareils de chauffage à combustion et n'obstruez jamais une aération d'air. Si vous suivez ces bonnes pratiques, vous diminuerez le risque d'intoxication au monoxyde de carbone. Cependant, afin de rendre l'espace encore plus sûr, équipez vos pièces avec des détecteurs de monoxyde de carbone. Faîtes les tester également à intervalles réguliers.
Résumer avec l'IA :























Si vous désirez une aide personnalisée, contactez dès maintenant l’un de nos professeurs !
Love you
Futur ingénieur, et la fibre enseignante…
Bravo !