
Le cuivre

La présence à l’état naturel de cet élément
Cuivre natif
Le cuivre est un métal assez abondant en certains points de la Terre. Son clarke s'élève à 60 g par tonne.
Le clarke d’un élément chimique définit sa présence moyenne dans la croûte terrestre . Il s’exprime sous la forme d’une fraction massique en pourcentage, ppm (partie par million), ou ppb (partie par milliard)
Il peut se trouver à l'état natif sous forme parfois de cristaux et plus régulièrement de fils, de feuilles et encore en recouvrement sur des minéraux. Il apparaît dans des espèces minérales telles que les basaltes, les grès et les schistes. On retrouve ces gisements naturels en plusieurs points de la Terre à savoir :
- En France (dans les Alpes notamment),
- Aux Etats-Unis,
- Au Canada,
- En Pologne,
- En Bolivie.
Cuivres gris
On trouve aussi du cuivre associé à de l'antimoine et de l'arsenic, c'est ce que l'on appelle des cuivres gris. Ils sont sont présents dans la freibergite, la tennantite ou encore la tétraédrite
Sulfures de cuivre
On peut aussi trouver le cuivre à l'état naturel sous forme de sulfures, dans les minéraux suivants :
- La chalcopyrite,
- La bornite,
- La covelline,
- La chalcocite,
- La carrollite,
- La germanite,
- La stannite,
- La kërsterite.
En chimie, un sulfure est un composé chimique où le soufre, sous sa forme S-2, donc en état d'oxydation -2, est associé à un autre élément chimique ou un de ses radicaux
Forme d'oxydes
Le cuivre s'oxyde sous la forme d'ions cuivriques de formule Cu2+ ou d'ions cuivreux de formule Cu+. On les retrouve dans les minéraux suivants : la cuprite et la ténorite.
Gisements
Il existe des mines de cuivre à ciel ouvert, où il se trouve sous la forme de sulfures en grande partie. Ses mines se trouvent en divers points du globe comme au Mexique, aux Etats-Unis, au Chili et au Pérou par exemple.
Le Nickel

Les ions du nickel en solution aqueuse
L'ion nickel II, de formule Ni2+, est un cation portant deux charges excédentaires positives, colorant sa solution aqueuse en vert. Il peut provenir de la dissolution sels tels que le chlorure de nickel, le sulfate de nickel ou le nitrate de nickel. En en milieu basique il forme un précipité verdâtre, mais en présence d'un excès d'ammoniac ce précipité se dissout et l'ion nickel forme un complexe bleu.
Extraction du nickel
Les méthodes d’extraction du nickel sont complexes et coûteuses, ce qui explique le prix parfois élevé de cette matière. Étant le plus souvent retrouvé dans la nature mélangé avec d’autres minerais tels que le fer ou le cuivre, il est nécessaire de séparer ces minerais afin d’exploiter le nickel. On peut alors utiliser une méthode de séparation chimique ou de séparation mécanique pour séparer la majeure partie des minerais. Afin d’obtenir une séparation plus fine, et donc un minerai plus pure, il est nécessaire d’effectuer un affinage par électrolyse ou par décomposition du nickel carbonylé.
L'alliage
Le cupronickel, également appelé cupro-nickel, correspond à un alliage constitué majoritairement de cuivre, de nickel pour 10 à 30% de sa masse mais également de fer en très faible proportion et d'autres éléments considérés comme des renforçateurs de résistance mécaniques comme le manganèse ou encore le silicium, le zinc, l'étain ou l'aluminium. Incontournable grâce à sa grande résistance à la corrosion, le cupronickel présente un grand nombre de débouché technique de par sa résistance à l'usure, à l'eau de mer ou encore plus largement aux milieux salins.
| Alloy UNS No. | Nom commun | Dénomination européenne | Ni | Fe | Mn | Cu |
|---|---|---|---|---|---|---|
| C70600 | 90-10 | CuNi10Fe | 9-11 | 1-1,8 | 1 | Reste jusqu'à 100% |
| C71500 | 70–30 | CuNi30Fe | 29–33 | 0,4-1,0 | 1 | Reste jusqu'à 100% |
| C71640 | 66–30–2–2 | 29–32 | 1,7-2,3 | 1,5-2,5 | Reste jusqu'à 100% |
Les propriétés du cupronickel
Cet alliage, lorsque le nickel constitue plus de 15% de la masse, présente un aspect brillant argenté. De plus, malgré que le nickel soit ferromagnétique, les éléments composés de cet alliage comme les pièces de monnaie ne sont pourtant pas soulevées par un aimant ordinaire.
Un élément est dit ferromagnétique quand il possède des propriétés de ferromagnétisme. Le ferromagnétisme est le mécanisme par lequel des matériaux forment des aimants permanents ou sont attirés par d’autres aimants. Le cobalt, le nickel ou encore le fer sont des éléments ferromagnétiques
Mais cet alliage présente d'autres propriétés très intéressante telles qu'une excellente ductilité après avoir été recuit mais également une bonne conductibilité thermique et d'autres bonne caractéristiques mécaniques telles que la résistance à la traction ou encore une dilatation thermique qui est adaptée à la réalisation de condenseur.
Un corps est dit ductile quand il peut être étiré sans pour autant se rompre
Toutes ces propriétés font de cet alliage un parfait candidat pour l'application de techniques cryogéniques.
| Alliage | Masse volumique g/cm3 | Conductivité thermique W/(m·K) | Dilatation thermique µm/(m·K) | Résistivité µOhm·cm | Module élastique GPa | Limite d'élasticité MPa | Résistance à la traction MPa |
|---|---|---|---|---|---|---|---|
| 90–10 | 8,9 | 40 | 17 | 19 | 135 | 105 | 275 |
| 70-30 | 8,95 | 29 | 16 | 34 | 152 | 125 | 360 |
| 66-30-2-2 | 8,86 | 25 | 15,5 | 50 | 156 | 170 | 435 |
Les usages des cupronickels
La plupart des cupronickels sont employés afin de fabriquer des objets utilitaires, résistants, stables tout en ayant un bel aspect. Cela est notamment le cas dans l'industrie d'armement, les industries électriques, chimiques et pétrochimiques tout comme pour divers objets d'ornementation. Mais le cupronickel est surtout d'un alliage commun de frappe monétaire. En effet, il est très souvent utilisé pour la fabrication de nombreuses pièces de monnaie. C'est notamment le cas des pièces de monnaie de la Confédération suisse. Mais cet alliage est également utilisé dans les milieux marins, en génie maritime et dans les unités de désalinisation grâce à sa résistance aux milieux salin. En effet, on le retrouvera dans les conduits et tuyauteries, les condenseurs et échangeurs de chaleur utilisant l'eau de mer, tout comme dans les équipements embarqués sur les bateaux, les hélices, les vilebrequins, les coques des navires performants comme les remorqueurs, les navires de pêches et autres vaisseaux de haute mer.
Exercice : le mélange entre des molécules de cuivre et des molécules de nickel

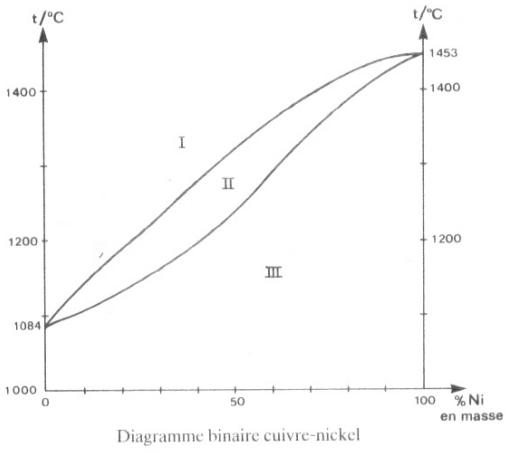
- Quelles sont les températures de fusion du cuivre et du nickel ?
- Donner les noms les deux courbes. Pour chaque domaine, décrire l'état du mélange et déterminer la variance.
- Un mélange liquide de cuivre et nickel commence à se solidifier à 1300 °C. Quelle est la composition de la dernière goutte qui disparaît ?
- On réalise un mélange liquide à 1500 °C de 587 g de nickel et 635 g de cuivre.
- Tracer l'allure de la courbe de refroidissement à P = 1 bar.
- Quelles sont les compositions des premiers et derniers cristaux solidifiés ?
- Quelles sont les masses de cuivre et nickel dans les phases liquides et solides à 1250 °C ?
Masses molaires atomiques : MNi = 58,7 g.mol-1 ; MCu = 63,5 g.mol-1
Résumer avec l'IA :























Si vous désirez une aide personnalisée, contactez dès maintenant l’un de nos professeurs !
Quelle est l’alliage équivalent à ASTM b171 alloy 715 en norme européenne, svp ?