
L'état gazeux
Toute entité chimique existe sous trois états possibles : solide, liquide ou gazeux, en fonction des conditions de température et pression. Chaque composé chimique possède pour une pression donnée, une température au delà de laquelle il devient gazeux (exemple : 100°C pour l'eau à pression atmosphérique). Les propriétés physico-chimiques du composé chimique sont dépendantes de son état, solide, liquide ou gazeux. A l'état gazeux, contrairement aux états solides et liquides, les molécules sont espacées et ont de faibles interactions les unes avec les autres. C'est également le seul état où la matière est dite compressible : l'espacement des molécules les unes par rapport aux autres peut être réduit afin qu'une même quantité de gaz prenne moins de place (exemple : les déodorants compressés qui durent aussi longtemps que le déodorant classique).
Qu'est-ce qu'un gaz parfait ?
Un gaz est dit parfait quand les interactions entre les différentes molécules peuvent être considérées comme nulles.
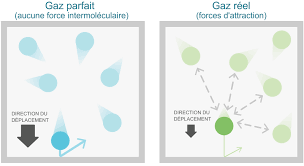
Comme le montre le schéma ci-dessus, dans le cas d'un gaz réel, les molécules interagissent plus ou moins entre elles suivants leur nature. Toutefois, dans des conditions de pression inférieures 10 atm (pression atmosphérique : 1 atm), les gaz réels ont un comportement que l'on peu assimiler à des gaz parfaits. En effet, les interactions intermoléculaires sont négligeables en raison de l'espacement important entre les molécules. La suite de cet article traitera uniquement du comportement de gaz parfaits ou de gaz réels considérés comme tels...
L'étude des propriétés physiques des gaz dans l'histoire
Les lois physiques décrivant le comportement des gaz ont été énoncées entre les milieux des XVIIe et XVIIIe siècles, suite aux observations faites les scientifiques de l'époque :
- Robert Boyle, physicien et chimiste irlandais (1627- 1691) : suite à des expériences relatives aux comportements physique des gaz, énonce en 1662 la loi appelée aujourd'hui de Boyle-Mariotte. Ces expériences l'amène également à penser que la matière résulte d'un ensemble de particules primaires. Il est un précurseur de la théorie des atomes par une approche expérimentale.
- Edme Mariotte, physicien et botaniste français (1620-1684) : découvre en 1676 au cours de ses expériences, indépendantes de celles de Boyle, la compressibilité des gaz et énonce la même loi que Boyle.
- Amedeo Avogadro, physicien et chimiste de Sardaigne (1776-1856) : constate que les comportements physique des gaz ne dépendent pas de leur nature et que dans les mêmes conditions, deux gaz de même volume contiennent le même nombre de molécules. Au cours de ses travaux, il distingue pour la première fois, l'atome et la molécule.
- André-Marie Ampère, mathématicien, physicien, chimiste et philosphe français ( 1775-1836) : parallèlement à Avogradro, il soutient que le volume d'un gaz est proportionnel au nombre de molécules qu'il contient. En découle aujourd'hui la loi au nom de ces deux chercheurs.
A noter que ces découvertes, à l'époque empiriques, donc basées sur l'observation et l'expérience, sont aujourd'hui démontrées grâce aux connaissances et aux techniques disponibles en physique-chimie.
La loi de Boyle-Mariotte
La loi de Boyle-Mariotte indique que si la température d'un gaz et sa quantité de matière sont constantes, alors le produit de sa pression (P) par son volume (V) est une constante. Cette loi peut se résumer par la relation suivante : PV = Constante à condition que T et n ne changent pas
- Avec P la pression,
- V le volume,
- T la température
- Et n la quantité de matière.
Conséquences de la loi de Boyle-Mariotte
Dans les conditions ou cette loi est valable :
- Si le volume diminue alors la pression augmente (on retrouve le résultat obtenu pour une compression).
- Inversement, si le volume augmente la pression diminue (on retrouve cette fois le résultat correspondant à une détente).
- Si la pression augmente alors il y a une diminution de volume.
- Inversement, si la pression diminue alors le volume augmente.
Utilisation de la loi de Boyle-Mariotte
Cette loi peut être utilisée pour trouver la nouvelle valeur de la pression lorsqu'il y a un changement de volume, ou inversement, pour trouver le nouveau volume s'il y a un changement de pression. Si la pression et le volume sont initialement de P1 et de V1 et que suite à une modification ils prennent les valeurs P2 et V2 alors, si les conditions d'utilisation de la loi de Boyle-Mariotte sont vérifiées, le produit de la pression par le volume du gaz étant constant, la relation suivante peut être écrite :  Si l'on cherche la nouvelle valeur de la pression on l'obtient en grâce à la relation :
Si l'on cherche la nouvelle valeur de la pression on l'obtient en grâce à la relation : 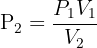 Si c'est la nouvelle valeur du volume qui est recherchée, on l'obtient en grâce à la relation :
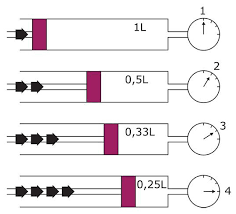
Si c'est la nouvelle valeur du volume qui est recherchée, on l'obtient en grâce à la relation : 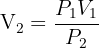 Ces relations montrent que si la pression est multipliée par deux alors le volume est divisé par deux, si la pression est multipliée par trois alors le volume est divisé par trois etc. Cela signifie que le volume est inversement proportionnel à la pression.
Ces relations montrent que si la pression est multipliée par deux alors le volume est divisé par deux, si la pression est multipliée par trois alors le volume est divisé par trois etc. Cela signifie que le volume est inversement proportionnel à la pression.
La loi d'Avogadro-Ampère
La loi d'Avogadro-Ampère spécifie que si deux gaz sont dans des conditions identiques de température et de pression, alors des quantités identiques de ces gaz occupent des volumes égaux, quelque soit leur nature.
Conséquences de la loi d'Avogadro-Ampère
La nature d'un gaz n'ayant pas d'influence sur le volume occupé : tous les gaz ont le même volume molaire. Cela signifie que, dans les mêmes conditions, les volumes occupés par une mole de deux composés chimiques sont identiques.
| Température degrés celsius/Kelvin Pression atmosphérique 1 atm | 0°C / 273 K | 25°C / 298 K | 50°C / 323 K | 100°C / 373 K |
|---|---|---|---|---|
| Volume molaire L/mol | 22,41 | 24,5 | 26,5 | 30,6 |
| Pression en atm Température 298 K | 1 atm | 2 atm | 3 atm | 4 atm |
| Volume molaire L/mol | 24,5 | 12,5 | 8,2 | 6,1 |
Utilisation de la loi d'Avogadro-Ampère
Cela peut se traduire, à température et à pression constante, par la relation suivante : 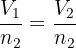
- avec V le volume,
- n la quantité de matière.
Ainsi, il est possible de comparer deux gaz afin de connaitre la quantité de matière de l'un, lorsque celle du second est connue : 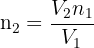
Conséquence du comportement des gaz sur le corps humain : la surpression pulmonaire
Qu'est ce que la surpression pulmonaire ?
C'est un phénomène, qui peut se produire lorsqu'un plongeur débutant remonte trop rapidement à la surface sans expirer. Les dommages subits sont sérieux voire mortels. Lors de la remontée, les poumons se dilatent jusqu'à atteindre leur volume maximal. Si le gaz contenu dans les poumons n'est pas expulsé des dommages seront engendrés :
- fissuration alvéolaires,
- pneumothorax...
Il est également possible pour soulager les poumons que l'air circule alors vers les vaisseaux sanguins, entraînant ainsi une embolie.
Comment expliquer ce phénomène avec la loi de Boyle-mariotte ?

Les poumons possèdent une certaine élasticité afin d'être capable d'emmagasiner et d'expulser l'air respiré. L'air contenu dans les poumons est à même pression que celle du milieu qui l'entoure. Celle-ci dépend pour le plongeur de la profondeur à laquelle il se situe. En effet, l'eau exerce un poids sur le plongeur, et plus ce dernier est en profondeur, plus le volume d'eau exerçant un poids est important, plus la pression est élevée :
- A la surface : c'est la pression atmosphérique de 1 atm.
- A 10 m : la pression est alors de 2 atm.
D'après la loi de Boyle-Mariotte, lorsqu'il descend de 0 à 10 m, le plongeur voit le volume de ses poumons remplis d'air passer de 5 L à 2,5 L (si le plongeur n'inspire ni expire). Par contre, comme l'indique la loi d'Avogadro-Ampère, la quantité d'air qu'ils contiennent ne varie pas (compressibilité d'un gaz). Ainsi, le plongeur à 10 m de profondeur pourra, en inspirant très profondément, remplir ses poumons avec plus d'air qu'à la surface, tout en atteignant le volume maximal de 5 L. Si ce plongeur remonte trop rapidement sans expirer, alors ses poumons, à l'image d'un ballon de baudruche, vont se dilater brutalement, et devront être capables de contenir 10 L d'air (la pression sera cette fois divisée par deux).
Résumer avec l'IA :






















Si vous désirez une aide personnalisée, contactez dès maintenant l’un de nos professeurs !
Très important cet article
j’aime bcp ce siteles explication sont tres bien donné et la encore sa c’es verifier vraiment merci bcp a mr Yann pour cette belle explication sur les gaz parfaits
Merci pour votre commentaire ! :)
Beaucoup de connaissance s’y trouvent vraiment merci
bon article il présenté le phénomène étudié d’une manière très pédagogique
Très intéressant et bien détaillé
Merci Diane! :)