Chapitres
| La première partie porte sur les ondes progressives créées |
Cet exercice se compose de deux parties indépendantes.
Certaines aides au calcul peuvent comporter des résultats ne correspondant pas
au calcul à effectuer.

A. Partition lunaire
Des chercheurs du CEA de l'équipe d'Elisabeth
Blanc viennent
d'annoncer qu'une éclipse n'a pas pour seul effet une baisse de la
luminosité.
Lors de l'éclipse du Soleil du 11 août 1999, à 12 h 16 précises,
l'ombre de la Lune commence sa traversée de la France à la vitesse de
2850 km.h-1 sur un axe Cherbourg-Strasbourg. Sur son passage, la température de l'air
chute rapidement d'environ 5°C. Le déplacement de cette zone froide, à la même
vitesse que celui de l'ombre (...), engendre dans son sillage des ondes
transversales dont la fréquence est largement inférieure à 20Hz.
D'après la revue Les Défis du CEA - n°97
octobre-novembre 2003.
1. Ondes créées lors de l'éclipse
1.1. Définir une onde mécanique progressive.
1.2. Définir une onde transversale.
1.3. Dire, en justifiant la réponse, si les ondes
créées lors de l'éclipse peuvent être sonores.
2. Caractéristiques des ondes créées
L'équipe en charge du projet a pu détecter à faible
altitude, une série d'ondes dont la période moyenne est de l'ordre de 10
minutes et la célérité moyenne est de l'ordre de 100 km.h-1.
2.1. Vérifier que la fréquence de l'onde est
effectivement largement inférieure à 20Hz.
2.2. Ces ondes peuvent-elles être diffractées par des
montagnes séparées par une distance de 10 km ? Justifier la réponse.
| Aide au calcul | |
|
|
|
B. Découverte historique d'un nouvel élément chimique
Lors de l'éclipse totale du Soleil du 18 août 1868, le
français Pierre Janssen et le britannique Norman Lockyer ont analysé le spectre
de la couronne solaire et ont remarqué qu'il présentait une raie brillante dans
le jaune très proche de celle du sodium. N. Lockyer a émis l'hypothèse que
cette raie était due à un nouvel élément qu'il baptisa hélium (du grec hélios
qui signifie Soleil). Ce n'est que vingt-sept ans plus tard que cet élément
chimique fut identifié sur Terre.
Données :
Célérité de la lumière dans le vide : c = 2,998 × 108
m.s-1
Constante de Planck : h = 6,626 × 10-34
J.s
1 eV = 1,602 × 10-19 J
Longueur d'onde de la raie D du sodium dans le vide : λNb = 589,0 nm.
Longueur d'onde de la raie jaune de l'hélium dans le vide : λHe =
587,6 nm.
| Aide au calcul | |
1. Spectre d'énergie
1.1. Illustrer, en s'aidant d'un schéma de niveaux
d'énergie d'un atome, le phénomène d'émission d'un photon (quantum d'énergie
lumineuse).
1.2. On note E l'énergie du photon émis lors d'une
transition énergétique d'un atome.
Donner l'expression littérale de E en fonction de la longueur d'onde λ de
la radiation lumineuse émise dans le vide, de la constante de Planck h
et de la célérité de la lumière dans le vide c.
1.3. Raie D du sodium
1.3.1. Calculer la valeur de E en
électronvolts, pour le rayonnement correspondant à la raie D du sodium.
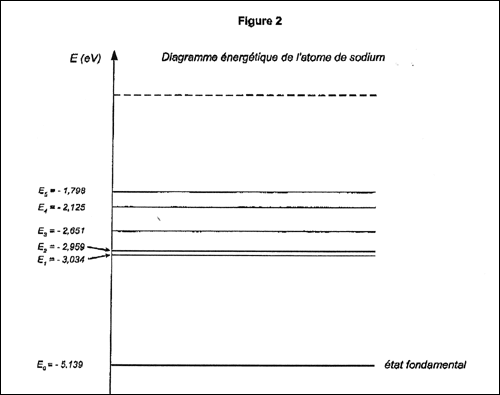
1.3.2. Déterminer, en s'aidant de la
figure ci-dessous, à quelle transition correspond cette émission.
1.4. L'énergie du photon correspond à l'émission de
la raie jaune de l'hélium (de longueur d'onde λHe) est égale à
2,110 eV. En s'aidant de la figure ci-dessous, justifier que cette émission ne
peut pas être attribuée au sodium.
2. Formation de l'hélium dans le Soleil
Les noyaux d'hélium 3 et d'hélium 4 peuvent être produits
par une suite de réactions nucléaires dont les équations sont indiquées ci-dessous :
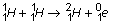
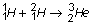
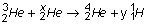
2.1. Quel nom donne-t-on à ces réactions
nucléaires ?
2.2. Parmi les noyaux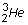
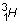
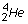
isotopes ? Justifier.
2.3. Déterminer les valeurs de x et y
dans la troisième équation de réaction et justifier la réponse en précisant les
lois de conservation utilisées.
2.4. On étudie dans la couronne solaire les spectres
d'émission des atomes d'hélium 3 et d'hélium 4.
On rappelle qu'un spectre atomique caractérise la configuration électronique de
l'atome (c'est-à-dire le nuage d'électrons de l'atome).
2.4.1. Ces deux types d'atomes
possèdent-ils la même configuration électronique ? Justifier.
2.4.2. Ces deux atomes auraient-ils
pu être distingués l'un de l'autre expérimentalement dans le spectre obtenu par
Pierre Janssen et Norman Lockyer ?
Résumer avec l'IA :























Si vous désirez une aide personnalisée, contactez dès maintenant l’un de nos professeurs !