
Définition d'objets chiraux
La chiralité est une notion qui s'applique aux objets en trois dimensions qui nous entourent.
Un objet est chiral s'il ne peut pas se superposer à son image dans un miroir.
Remarque : "l'image dans un miroir" d'un objet correspond également à son symétrique par rapport à un plan.
Un exemple simple d'objet chiral est la main humaine : l'image de la main droite dans un miroir correspond à la main gauche et réciproquement. Cependant les deux mains ne peuvent se superposer.
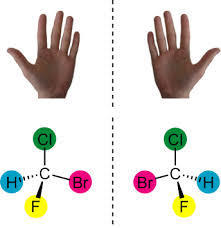
Un objet qui peut se superposer à son image dans un miroir est quant à lui qualifié d'achiral. Un ballon de foot est par exemple un objet achiral.
La chiralité des molécules
La notion de chiralité s'applique également aux molécules en trois dimensions. En revanche, une molécule plane (double liaisons carbone-carbone par exemple) ne peut être chirale.
Les deux formes chirales d'une molécule, sont appelées énantiomères. Aussi proches soient-elles ces molécules peuvent avoir des propriétés différentes.
Particularités des molécules chirales
Déviation de la lumière polarisée par une molécule chirale
Les molécules chirales ont la propriété de dévier la lumière polarisée. L'un des isomères la dévie vers la droite, l'autre vers la gauche.
C'est cette propriété qui a permis à Pasteur de différencier le L-acide tartrique du D-acide tartrique.
Propriétés physico-chimiques des molécules chirales
Deux énantiomères possèdent des propriétés physico-chimiques identiques : mêmes masses moléculaires, mêmes solubilités, mêmes points de fusion et d'ébullition, ce qui les rend difficiles à séparer et identifier.
Cependant, de leurs configurations spatiales particulières, les interactions avec d'autres molécules chirales seront différentes.
Propriétés biologiques des molécules chirales
Comme décrit plus tôt, les énantiomères chiraux ont des géométries spatiales opposées et donc peuvent interagir différemment avec leur environnement. Cette particularité a une grande importance en parfumerie et encore plus pharmacologie.
En effet, deux énantiomères n'auront pas nécessairement la même activité biologique car ils ne réagiront pas avec les mêmes récepteurs.
C'est le cas du limonène, présent en abondance dans les huiles essentielles d'agrume, qui possède un énantiomère à l'odeur de citron et l'autre à l'odeur d'orange. De la même manière, pour les molécules médicales, il n'est pas rare qu'un énantiomère ai des propriétés bénéfiques tandis que l'autre est très toxique.
Ceci s'explique par les interactions entre les molécules et les récepteurs du corps humain fonctionnant comme des systèmes clefs-serrures : une forme rentre dans une serrure donnée et l'autre dans une autre, voire aucune, mais jamais dans la même en raison de leurs formes non superposables.

Molécules chirales synthétiques versus naturelles
La plupart du temps la nature fait un choix et ne produit qu'un seul énantiomère. Par exemple les acides aminés du corps humain et de la plupart des organismes vivants (pas nécessairement tous) sont L, tandis que les sucres (constituants important du règne végétal) sont principalement D.
Par contre, la chimie organique classique à tendance à produire les deux énantiomères en égale quantité, et produit ce que l'on appelle un mélange racémique. En effet, le plus souvent, les réactifs de départ sont achiraux, la réaction se produit alors indifféremment de chaque coté du plan. Cette différences entre la synthèse naturelles et celle au laboratoire a plusieurs conséquences :
- Difficultés à reproduire la nature à l'identique. Nous l'avons vu cela peut avoir des conséquences au niveau du goût, de l'odeur ou des propriétés pharmacologiques.
- Possibilité de différencier un produit contenant des molécules chirales synthétiques d'un produit en contenant des naturelles. Cela est intéressant dans le cadre de l'étude de fraudes notamment, en identifiant la présence d'un énantiomère non naturel (huiles essentielles déclarées à tort comme 100% naturelles).
Historique de la découverte des molécules chirales
Au début du XIXe, Jean-Baptiste Biot remarque pour la première fois que certaines molécules ont la capacité de dévier la lumière polarisée. Cette propriété est utilisée à l'époque pour mesurer la concentration de certains sucres dans l'eau.
C'est Louis Pasteur qui eut le premier l'intuition de l'existence de molécules chirales en 1848. En observant au microscope des cristaux de sels d'acide tartrique, grâce à sa grande expérience de la cristallographie, il remarqua qu'il en existait deux sortes, images l'un de l'autre dans un miroir, mais sans qu'ils soient superposables.
Pasteur fit donc l'hypothèse que la chiralité de ces cristaux était une conséquence de la chiralité des molécules qui les constituent.
Il sépare ensuite manuellement les cristaux selon leurs formes et mesure la déviation de la lumière de chacune des deux formes séparément. C'est ainsi qu'il remarque que l'une la dévie à droite et l'autre à gauche.
Il déduit de toute cette expérience que les cristaux sont constitués de deux molécules d'acides tartriques de géométries spatiales différentes, déviant la lumière polarisée dans des sens opposées. Il fait donc le lien entre chiralité et déviation de la lumière polarisée.
Comment savoir si une molécule est chirale ?
Il est possible de se référer à la définition initiale de la chiralité en déterminant le symétrique d'une molécule par rapport à un axe, puis en vérifiant si ce symétrique peut se superposer complètement à la molécule initiale.
Il est également possible d'utiliser un critère beaucoup plus simple : si une molécule ne comporte pas de plan de symétrie, alors elle chirale et si elle en comporte au moins un, elle est achirale.
Cependant, lorsque les molécules sont plus complexes, se référer à la définition n'est pas toujours évident. Il existe une autre façon de procéder, en utilisant la présence de carbones asymétriques.
Carbone asymétrique et chiralité
Un carbone est dit asymétrique à condition :
- qu'il comporte quatre liaisons simples.
- Que tous les atomes et groupes d'atomes auxquels il est lié soient différents les uns des autres.
Un carbone est donc asymétrique s'il est liés à quatre atomes ou groupes d'atomes différents. Dans une molécule un carbone asymétrique peut être distingué des autres en le notant avec une petite étoile en exposant (C*).
Ce type d'atome peut être utilisé dans certains cas pour savoir si une molécule est chirale : si elle ne comporte qu'un seul atome de carbone asymétrique alors cette molécule est chirale. Cependant, la présence de plusieurs carbones asymétriques dans une molécule n'indique pas forcément qu'elle est chirale.
Représentation spatiale des molécules chirales : la représentation de CRAM
Pour aborder la notion de chiralité des molécules, il est nécessaire de pouvoir représenter leur géométrie spatiale. Pour ce faire c'est la notation de CRAM qui est utilisée.
Cette notation présente l'atome de carbone comme central, et les 4 atomes le substituant sont positionnés selon les sommets d'un tétraèdre (voir schémas de molécules ci-dessous).
Pour l'atome en avant du plan, la liaison avec le carbone est représentée par un trait plein.
Pour l'atome en arrière du plan, la liaison avec le carbone est représentée en pointillés.
La nomenclature associée aux molécules chirales
Notation D et L des molécules chirales
C'est la notation historique. Cette nomenclature est directement liée au pouvoir rotatoire (déviation de la lumière polarisée) des molécules chirales. Les molécules déviant la lumière à droite sont dextrogyres et un D précède le nom de la molécule (acide D-tartrique). Les molécules déviant la lumière à gauche sont lévogyres et noté L en amont du nom de la molécule (acide L-tartrique).
Aujourd'hui, la notation (+) est souvent utilisée au lieu de D et (-) au lieu de L.
Notation R et S des molécules chirales
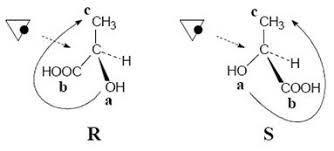
L'application de cette nomenclature a l'avantage de ne pas nécessiter d'analyses particulières. Ce sont les règles de Cahn Ingold et Prélog qui sont appliquées :
- Les atomes substituants au carbone asymétrique ont un ordre d'importance, plus le numéro atomique est grand, plus l'atome est important.
- Une fois l'ordre d'importance connu, on regarde dans quel sens il faut tourner pour aller de l'atome ou du groupement le plus important au moins important : dans le sens des aiguilles d'une montre, ou vers la droite, c'est R (comme rectus signifiant droit en latin), dans le sens inverse des aiguilles d'une montre, ou vers la gauche, c'est S (comme sinister signifiant gauche en latin)
- S'il existe plusieurs carbones asymétriques dans une même molécule, chacun sera défini selon la règle de Cahn Ingold et Prelog. La molécule aura autant de "R" ou de "S" que de carbones asymétriques.
- La mention "numéro carbone"R ou "numéro carbone"S précède le nom de la molécule. Ex : (-) menthol est le (1R,2S, 5R)-5-méthyl-2-isopropylcyclohexanol
A noter que ces deux nomenclatures ne sont pas liées et qu'un énantiomère R peut être indifféremment D ou L et inversement.
La notation R et S prévaut aujourd'hui en chimie, tandis que la L et D continue d'exister en biochimie (acides aminés). Cependant beaucoup de molécules chirales commerciales, n'ont pas changé de nom et continuent à être nommée avec la nomenclature L et D. Cela aussi pour des raisons pratiques car si la molécules possèdent de nombreux carbones asymétriques, la lisibilité est moindre avec la notation R et S.
L'analyse des énantiomères chiraux
Grâce à leurs géométries spatiales différentes, les énantiomères chiraux peuvent dans certaines conditions être séparés et/ou analysées.
A la manière de Pasteur, les molécules chirales peuvent être caractérisées par la mesure de la déviation de la lumière polarisée, en utilisant un appareil appelé polarimètre. Cependant, cette technique requiert l'analyse d'une solution contenant l'énantiomère pur.
Une technique très rependue pour l'analyse d'énantiomères, est la chromatographie chirale. En effet, en chromatographie classique, les énantiomères ne sont pas séparés et ne peuvent être quantifiés. La chromatographie chirale, quant à elle, joue sur les différentes forces d'interactions qu'ont les énantiomères avec des molécules elles-mêmes chirales. Ainsi, les énantiomères peuvent être séparés et quantifiés.
Plus récemment, la RMN a également permis des avancées dans l'analyse de molécules chirales. En effet, cette technique peut différencier des signaux de molécules chirales en les plaçant en solution dans des cristaux liquide chiraux, au lieu de solvant classique (eau, éthanol, dichlorométhane deutérés).
Conséquences de la chiralité dans l'industrie chimique
La chiralité est un enjeu majeur pour l'industrie pharmaceutique car comme évoqué précédemment :
- Au laboratoire, en utilisant une synthèse classique, les deux énantiomères sont synthétisés en égale quantité.
- Un des deux énantiomères possède l'activité pharmacologique recherchée tandis que l'autre est au mieux inactif, au pire toxique.
Par exemple, la méthamphétamine est disponible en pharmacie sous le nom de Vicks comme décongestionnant nasal (énantiomère L) mais est également bien connus par les fans de la série Breaking Bad comme drogue psychotrope synthétisée par Walter White. On comprend alors que le laboratoire pharmaceutique préparant le Vicks a intérêt à fabriquer un énantiomère L extrêmement pur !
Il existe également un exemple moins drôle dans les années 50-60 (et ce n'est malheureusement pas le seul), où la différence de propriétés pharmacologiques entre les énantiomères était moins connue ou sous-estimées : la thalidomide. Cette molécule a été un temps prescrit aux femmes enceintes pour soulager les nausées. Le médicament était constitué des deux énantiomères, et, si le L-thalidomide apporte les effets recherchés, la D-thalidomide provoque malheureusement des malformations fœtales.
Résumer avec l'IA :






















Si vous désirez une aide personnalisée, contactez dès maintenant l’un de nos professeurs !
Je cherche les avantages de la chiralité
Bonjour, nos talentueux professeurs sont disponibles pour toute aide personnalisée, n’hésitez pas à les solliciter. Excellente journée ! 🙂
C’est une merveille que d’avoir des explications magistrales en la matière. Merci pour l’éclairage , et aussi a Breaking-Bad.
Merci beaucoup! Vous m’avez permis d’être mieux éclairé sur ce sujet pendant ma préparation d’examen :)
Bonjour, merci pour votre gentil commentaire !
Bonsoir! Je voudrais avoir des exercices qui sont appropriés avec la theorie s’il vous plaît.
Excellent article, très simple et qui montre l’intérêt de certaines notions en chimie organiques qui sont malheureusement rarement présenté ainsi dans les cours magistraux. Pour avoir fait beaucoup de chimie organique sans rien comprendre…en lisant cette ressource, j’ai compris, pour la première fois, l’intérêt d’étudier la chiralité. Encore merci… espérant que, c’est de cette façon qu’on la présente aujourd’hui aux élèves et étudiants…