Chapitres

L'atome
Sa découverte
En 400 av JC, un philosophe grecque nommée Démocrite est le premier homme à penser que la matière est constitué de minuscules particules tellement petites que l'on ne peut les diviser d'où leur nom de atomos qui signifie indivisible en grec.
La première approche des électrons date de l'époque de la Grèce Antique. Ceux-ci avaient pris conscience qu'une certaine oléorésine, l'ambre était capable d'attirée des objets si elle était frottée avec de la fourrure. Sans le savoir, ils venait de découvrir l'électricité statique. Il s'agit du deuxième phénomène électrique dont l'Homme a pris conscience, juste après la foudre. En 1269, un ingénieur militaire qui servait auprès du prince Charles Premier de Sicile, se mit à étudier le phénomène d'attirance ente des petits objets après qu'ils aient été frottés.
La découvert de l'atome est imputable à Ernest Rutherford. Durant le début des années 1910, il s'est attelé à comprendre la composition de l'atome. Il a alors déterminé que l'atome était constitué d'un noyau qui concentrait toute la charge positive et aussi presque toute la masse de l'atome. Ce noyau est entouré d'un nuage électronique composé d'électrons. L'un de ses collègues de laboratoire, Niels Bohr, a quant à lui démontré que les états de l'électrons dépendaient de l'énergie déterminée par le nombre n de l'atome. C'est à lui qu'on doit la compréhension de l'émission d'un photon lors d'un passage à un état inférieur.

Ernest Rutherford
Ernest Rutherford est un physicien et chimiste néo-zélandais ayant vécu de 1871 à 1937. On le considère comme l’un des précurseurs de la physique nucléaire. On lui doit notamment la découverte :
- Des rayons alpha,
- Des rayons bêta,
- Du noyau atomique et de ses charges électroniques,
- De la désintégration nucléaire.
Toutes ses recherches le conduisirent à diriger le prestigieux laboratoire Cavendish de l’université de Cambridge au Royaume-Uni mais aussi de recevoir le prix Nobel de chimie en 1908.
Niels Bohr
Niels Henrik David Bohr est né le 7 Octobre 1885 à Copenhague et est mort le 18 novembre 1962 dans la même ville. Ce physicien danois est surtout connu pour sa contribution à l’établissement de la physique quantique. Il a d’ailleurs reçu pour cela de nombreux honneurs : il a même été lauréat du prix Nobel de physique en 1922 pour son développement des mécanique quantique. Mais avant cela, il a été en 1921, lauréat de la médaille Hughes. En 1926, il devient membre étranger de la Royal Society.
La Royal Society of London for the Improvement of Natural Knowledge, abrégée en Royal Society, est l’institution des sciences en Angleterre. Fondée en 1660 à Londres, elle est au Royaume-Uni l’équivalent de l’Académie des sciences en France.
Par la suite, il devient lauréat de la médaille Franklin, toujours en 1926. Il devient par la suite lauréat du Daraday Lectureship de la Société Royale de chimie en 1930 puis lauréat de la médaille de Copley en 1938. N’étant ni membre d’une famille royale, ni chef d’Etat, il deviendra en 1947 le troisième et dernier Danois à être admis au sein de l’Ordre de L’Élephant au cours du xxe siècle.
L’ordre de l’Éléphant est un ordre de chevalerie danois. La décoration représente un éléphant portant une tour. C’est un insigne en émail blanc qui est suspendu à un collier d’or ou à un ruban bleu passé de l’épaule gauche au côté droit.
Il deviendra par la suite président de l’Académie royale danoise des sciences et des lettres de 1939 à 1962. En son honneur, l’Union astronomique internationale nommera une vallée lunaire « la Vallis Bohr ».
Besoin d'un prof de physique chimie ?
Les caractéristiques de l'atome
Masse
La masse des électrons est négligeable devant celle du noyau.
On dit que la masse d'un atome est concentrée dans son noyau
Taille
La taille d'un atome est infiniment petite.
Le diamètre d'un atome vaut en moyenne 10-1 nm ( 1nm = 10 -9 m ).
Le diamètre du noyau vaut en moyenne 10-6 nm.
Le noyau est 100 000 fois plus petit que l'atome.
Entre les électrons et le noyau, il n'y a que du vide.
On parle de la structure lacunaire de l'atome.
Charge électrique
C'est la somme de la charge électrique + des particules du noyau et celle – des électrons.
Cette somme est nulle : On dit que l'atome est électriquement neutre.
Les charges électriques étant les même, il y a autant d'électrons qui gravitent autour du noyau que de particules le constituant.
Exemple : L'atome de fer a 26 électrons et 26 particules + dans son noyau.
Notion de couches électroniques
Cas de l'atome d'hydrogène
Nous avons déjà rencontré le modèle probabiliste de l'atome d'hydrogène (fiche "atome et élément"). Rappelons que dans ce modèle, les points présents sur le schéma représentent la probabilité de trouver l'unique électron de cet atome à un instant donné. L'électron a d'autant plus de chance de se trouver dans une région de l'espace autour du noyau qu'il y a de points dans cette zone. Il apparaît sur le schéma ci-contre une zone sphérique, centrée sur le noyau, d'épaisseur faible et de rayon moyen r=53pm, dans laquelle l'électron a de grandes chances de se trouver.
On dit que l'électron appartient à une couche dont le rayon moyen est 53pm.

Cas des autres atomes
Un atome quelconque possède Z électrons dans son cortège électronique. Comme pour l'atome d'hydrogène, les électrons d'un atome quelconque se répartissent autour du noyau sur de couches.
Les électrons d'un atome (ou d'un ion monoatomique) ne sont pas tous liés de la même façon au noyau. Ceux qui sont proches du noyau y sont très liés (par des forces), ceux qui en sont plus éloignés y sont moins liés.
Les électrons qui appartiennent à une même couche sont donc situés à la même distance moyenne du noyau et sont liés de la même façon à ce noyau.
La couche la plus proche du noyau est notée K, les suivantes sont notées dans l'ordre croissant d'éloignement: L, M, N, O, P, Q. Cette année nous ne considérerons que les trois premières couches.
Répartition des électrons d'un atome (ou d'un ion monoatomique)

La couche de valence
La couche de valence d'un atome est sa dernière couche électronique qui continent des électrons. Ce tableau récapitule les électrons de valence selon les groupes d'atomes :
| Groupe | Numéro de groupe | Nombre d'électrons de valence |
|---|---|---|
| Métaux alcalins | 1 | 1 |
| Métaux alcalino-terreux | 2 | 2 |
| 13 | 3 | |
| 14 | 4 | |
| Pnictogènes | 15 | 5 |
| Chalcogènes | 16 | 6 |
| Halogènes | 17 | 7 |
| Gaz nobles | 18 | 8 A exception de l'Hélium qui en a 2 |
Remarques
Etat fondamental
Les électrons peuvent être répartis de différentes façons dans les différentes couches. Les règles de répartitions données ci-dessous concernent ce que nous appellerons l'atome dans son état fondamental. C'est la seule répartition à connaître dans le programme de la classe de seconde.
Définitions
La couche la plus éloignée du noyau qui contient des électrons est appelée couche externe.
Les électrons de cette couche externe sont appelés électrons périphériques.
Règles de remplissage des couches électroniques
Première règle
Une couche électronique ne peut contenir qu'un nombre limité d'électrons.
- La couche K (première couche) peut contenir un maximum de 2 électrons (c'est-à-dire qu'elle peut contenir 0; 1 ou 2 électrons) ;
- La couche L (deuxième couche) peut contenir un maximum de 8 électrons (c'est-à-dire qu'elle peut contenir 0; 1;...;7 ou 8 électrons) ;
- La couche M (troisième couche) peut contenir un maximum de 8 électrons (seulement pour les éléments tels que Z<18).
Lorsqu'une couche est pleine on dit qu'elle est saturée.
Deuxième règle
Le remplissage des couches électroniques s'effectue en commençant par la couche K. Lorsqu'elle est saturée on remplit la couche L et ainsi de suite.
Répartition ou formule électronique d'un atome ou d'un ion monoatomique
Les règles de remplissage précédentes permettent d'établir la répartition électronique (ou formule électronique) d'un atome ou d'un ion atomique de la façon suivante:
- On détermine le nombre d'électrons à repartir (Z électrons pour un atome).
- On écrit, côte à côte et entre parenthèses, les lettres de chaque couche contenant des électrons.
- On indique, en haut et à droite de chaque parenthèse, le nombre d'électrons présents dans la couche considérée.
Exemple: pour un atome de carbone Z=6. Le noyau de cet atome possède donc 6 protons. Cet atome étant électriquement neutre, il possède 6 électrons qu'il faut répartir. En utilisant les règles précédentes, on établit la formule électronique du carbone. Soit: (K)2(L)4.
Quelques exercices
Le sucre et les électrons
Et si l’électricité prenait désormais sa source dans la nature grâce aux biopiles… Depuis dix ans, glucose, bactéries ou plantes inspirent les chercheurs en quête d’une source d’énergie alternative et propre.
Les avancées dans ce domaine se multiplient notamment pour des applications biomédicales nécessitant de faibles puissances électriques (alimentation d’un pacemaker par exemple).

En 2010, des chercheurs ont ainsi réussi à mettre au point une pile uniquement alimentée par le glucose de l’organisme. Ce dispositif de quelques millimètres permet au dioxygène et au sucre présents dans différents liquides physiologiques du corps de réagir. Cette réaction, qui génère des électrons, conduit à la production de courant par la pile. Le procédé, totalement naturel, est basé sur l’oxydation du glucose par le dioxygène, avec l’utilisation d’enzymes qui recouvrent les électrodes.
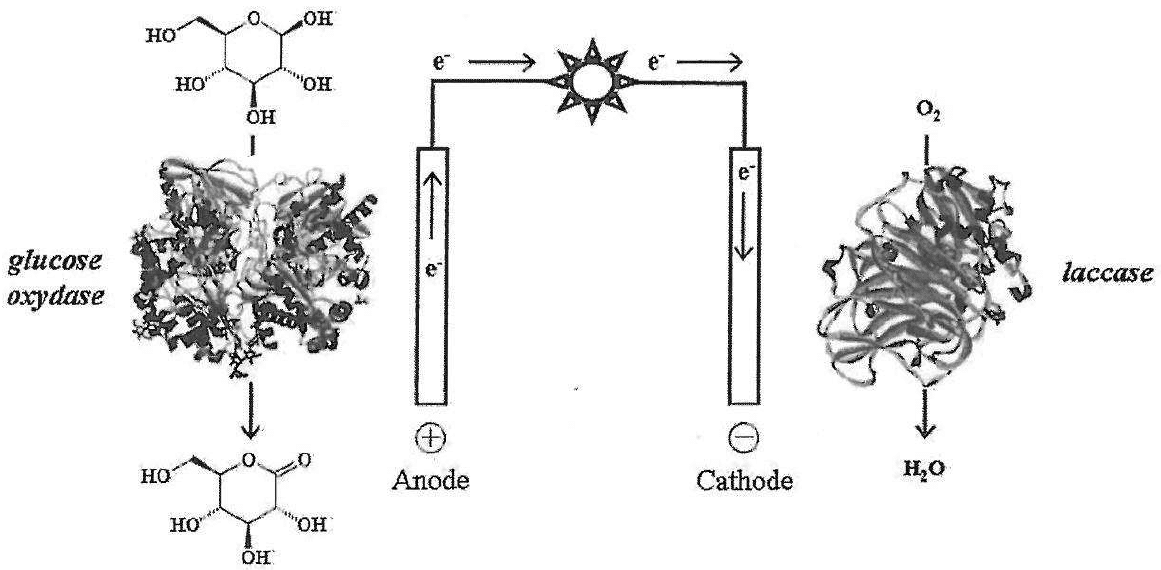
Réaction d’oxydation à l’anode : C6H12O6 → C6H10O6 + 2 H+ + 2 e–
Réaction de réduction à la cathode : O2 + 4 H+ + 4 e– → 2 H2O
Le glucose
Le glucose existe dans la nature sous deux formes : une forme linéaire, le D-glucose, et deux formes cycliques :
le a-D-glucopyranose et le b-D-glucopyranose.
Forme linéaire du glucose

Identifier sur l’ANNEXE à rendre avec la copie les groupes caractéristiques de cette molécule et nommer la fonction associée à chacun d’eux.
Sur la même représentation de la molécule de D-glucose (ANNEXE), identifier les atomes de carbone asymétrique.
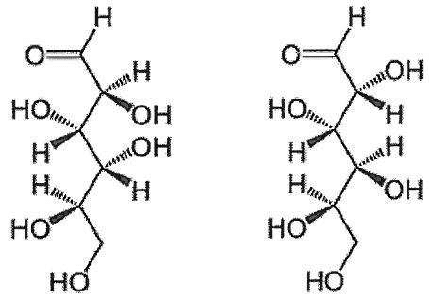
Deux stéréoisomères du glucose, le D-mannose et le D-galactose, existent dans la nature.
Sont-ils des énantiomères du D-glucose ? Justifier.
Forme cyclique du glucose
La représentation de Cram du b-D-glucopyranose est donnée ci-dessous.
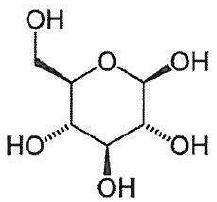
Les étapes du mécanisme de cyclisation permettant de passer de la forme linéaire du D-glucose à la forme cyclique, le b-D-glucopyranose, sont données ci-après.
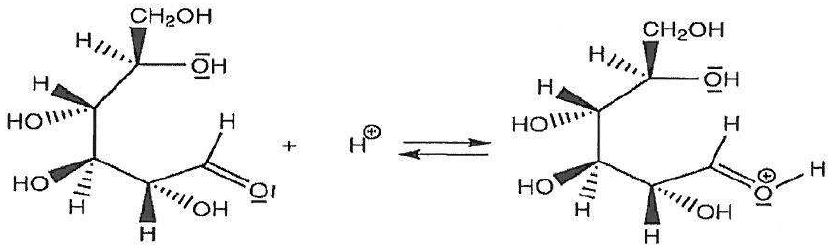
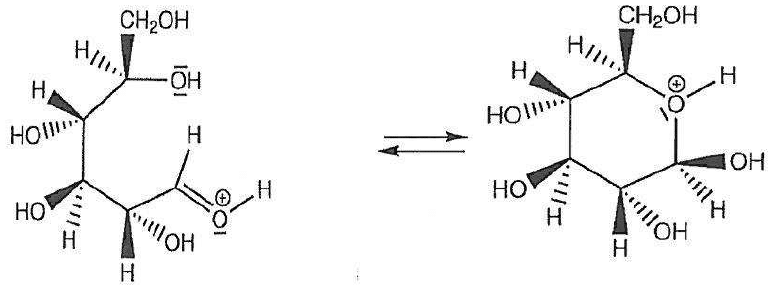
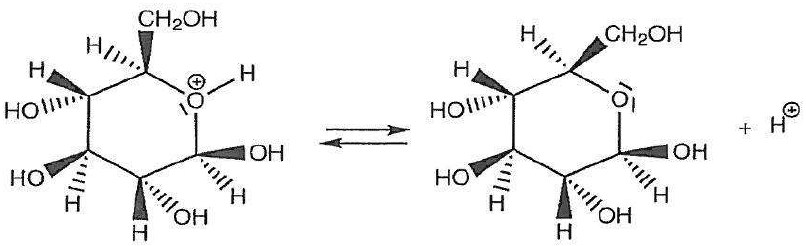
Sur l’annexe à rendre avec la copie, identifier le site donneur et le site accepteur mis en jeu dans l’étape n°2, et représenter les flèches courbes rendant compte de cette étape.
La cyclisation est d’autant plus rapide que la concentration en ion H+ est importante.
Peut-on considérer que l’ion H+ est catalyseur de cette réaction ?
Justifier.
Rôle de l’enzyme glucose oxydase dans l’oxydation du glucose
Pour illustrer les effets de l’enzyme glucose oxydase, des élèves réalisent quatre suivis cinétiques de l’oxydation du glucose par le dioxygène. Ils réalisent quatre mélanges identiques de solution de glucose et de dioxygène, le dioxygène étant le réactif limitant.
Les courbes donnant la concentration en dioxygène dans le milieu en fonction du
temps pour chaque expérience sont représentées ci-après.
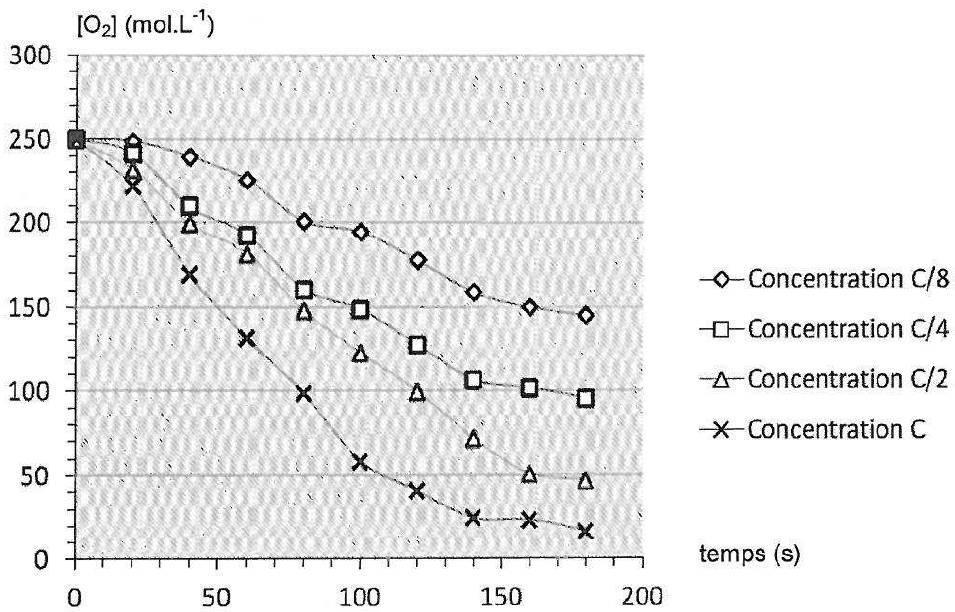
Écrire l’équation de la réaction d’oxydation du glucose par le dioxygène, sachant que les couples oxydant/réducteur mis en jeu sont C6H10O6/C6H12O6 et O2/H2
Quel est le rôle de la glucose oxydase dans la réaction d’oxydation du glucose par le dioxygène ? Justifier.
Représenter qualitativement, sur l’annexe à rendre avec la copie, l’allure de la courbe donnant l’évolution de la concentration en dioxygène dans la solution en l’absence de glucose oxydase.
Comment évolue le temps de demi-réaction en fonction de la concentration en enzyme ? Justifier graphiquement sur annexe à rendre avec la copie.
Dans la biopile au glucose, l’oxydation du glucose a lieu à l’anode et la réduction du dioxygène, à la cathode.
L’intensité du courant étant d’autant plus grande que le débit d’électrons dans le circuit est important, que peut-on dire de l’évolution de l’intensité du courant en fonction de la concentration en glucose oxydase ?
En réalité, l’enzyme est opérante uniquement sous la forme cyclique principale du glucose, le b-D-glucopyranose, et inopérante sous la forme linéaire du glucose ou sur l’autre forme cyclique du glucose, le α-D-glucopyranose.
Quelle caractéristique de sa réactivité cela illustre-t-il ?
Durée de fonctionnement de biopiles
L’obstacle majeur d’un développement à large échelle des biopiles reste leurs dimensions. Pour alimenter de gros appareils, il faut en effet en associer un grand nombre.
À titre d’exemple, l’entreprise Sony a commercialisé un lecteur mp3 nécessitant une puissance d’alimentation égale à 150 mW alimenté par une pile composée de sucre et d’eau. La pile avait une longueur d’environ 20 cm (voir photo ci-contre) et une réserve de 100 g de glucose.
Données :
énergie libérée par la réaction du glucose et du dioxygène dans la biopile :
150 kJ par mole de glucose oxydé ;
énergie E (en joule) reçue par le lecteur mp3 pendant la durée Dt (en seconde) :
E = P . Dt où P (en watt) est la puissance d’alimentation.
Déterminer la durée de fonctionnement du lecteur mp3 alimenté par la biopile au glucose commercialisée.
On trouve du glucose dans les fruits, ce qui fait des jus de fruits un moyen de recharger les biopiles. L’étude qui suit a pour objectif d’évaluer l’énergie disponible dans une biopile au glucose rechargée avec un litre de jus de raisin.
On introduit dans une fiole jaugée de 50 mL, 2,0 mL de jus de raisin et 20,0 mL d’une solution de diiode (coloration jaune en milieux aqueux) de concentration 2,0 × 10–2 mol.L-1. La fiole est complétée par une solution d’hydroxyde de sodium. La réaction qui se produit lors du mélange a pour équation chimique :
I2(aq) + 3 HO–(aq) + RCHO(aq) → RCOO–(aq) + 2 H2O + 2 I–(aq)
Les ions hydroxyde et le diiode sont introduits en excès.
Le glucose est noté RCHO.
Une fois la réaction terminée le diiode en excès est dosé par spectrophotométrie, l’appareil est réglé à la longueur d’onde de 440 nm : la mesure de l’absorbance d’un échantillon de la solution donne A = 1,6.
Une courbe d’étalonnage a été tracée à cette longueur d’onde à partir de quatre solutions de concentration connue en diiode.

Déterminer la durée de fonctionnement du mp3, alimenté par une pile au glucose composée d’un litre de ce jus de raisin.
Le candidat est invité à présenter la démarche suivie, même si elle n’a pas abouti. Toute prise d’initiative sera valorisée.






















Si vous désirez une aide personnalisée, contactez dès maintenant l’un de nos professeurs !