
Les différents changements d'états
Il existe 3 états élémentaires de la matière auxquels on peut ajouter un quatrième :
- Solide ;
- Liquide ;
- Gazeux ;
- Plasma.

L'état solide est l'état le plus "serré" de la matière. En effet, toutes les molécules sont collées les unes au autres, c'est ce qui donne à l'élément sa solidité. L'état liquide est un intermédiaire entre l'état solide et l'état gazeux. La matière y est malléable et coule. L'état gazeux est l'état dans lequel la matière est la plus dissipée. En effet, un gaz occupe toute la place qu'on lui offre, ce qui signifie qu'il peut s'étendre. Le plasma apparaît dans des conditions de température et de pression extrêmes. Dans ces conditions, même la structure atomique est totalement désorganisée. Ainsi, dans l’état de plasma, les constituants de l'atome se séparent. Les noyaux et les électrons se déplacent indépendamment et forment un mélange globalement neutre. Cet état de neutralité en fait l’état le plus important de l’Univers : le plasma représente près de 90% de la matière visible.
Les changements d'états
Il existe en tout 6 changements d'états possibles. Ce sont les six transformations fondamentales qui interviennent en chimie. Nous prendrons pour les détailler l'exemple de l'eau.
La condensation solide
La condensation solide est le phénomène qui se produit lorsque de l'eau sous forme de vapeur vient toucher une surface très froide. Par exemple, si l'on souffle sur une vitre gelée, la vapeur d'eau contenue dans notre respiration gèlera instantanément en se transformant en eau solide.
La vaporisation
La vaporisation est le passage de l'état liquide à l'état gazeux. Même si le nom est proche, cela n'a aucun rapport avec le fait de projeter de l'eau avec un vaporisateur. La vaporisation a lieu lorsqu'on laisse évaporer de l'eau au soleil ou quand on la porte à ébullition.
La solidification
La solidification est le phénomène durant lequel l'eau liquide devient solide. Cela se produit quand elle gèle, on parle alors de congélation. L'eau se met à se solidifier une fois qu'elle descend en dessous de 0° C. L'eau peut aussi se solidifier en cas de cristallisation ou d'augmentation de la pression.
La fusion
La fusion intervient lorsque de la glace fond. Par exemple, un glaçon dans un verre d'eau. Il s'agit donc du passage de l'état solide à l'état liquide.
La sublimation
La sublimation intervient quand l'eau passe directement de l'état solide à l'état gazeux. Cela fait que la glace devient vapeur sans même passer par les étapes habituelles de fusion et de vaporisation. Cela peut arriver lorsque de l'eau très chaude entre en contact avec de l'air très froid. Elle part alors en fumée blanche (de la vapeur d'eau).
La liquéfaction
Il s'agit de la transformation inverse de la vaporisation. Elle intervient quand de la vapeur d'eau se transforme en eau liquide. La liquéfaction a lieu soit par compression : la pression qui augmente rends l'eau gazeuse liquide ou par refroidissement et dans ce cas le gaz refroidit pour devenir liquide, c'est la condensation.
L’ébullition de l’eau

Expérience
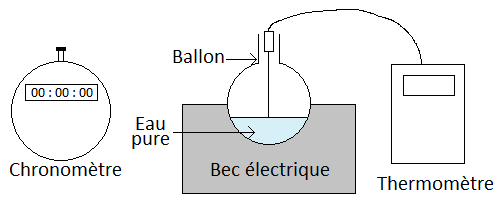
Nous obtenons alors ce graphique :
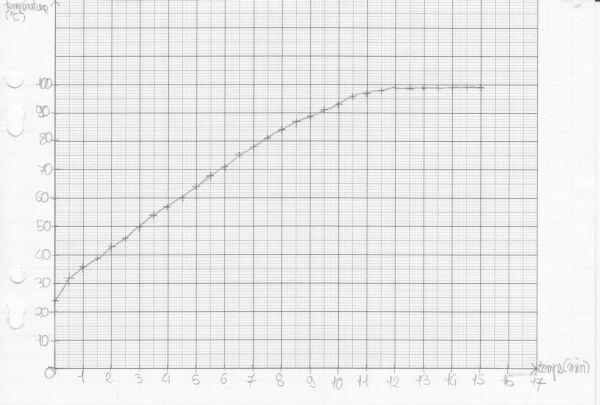
Conclusion
L’eau pure passe de l’état liquide à l’état gazeux (vaporisation) à la température de 100°C. Pendant toute la durée du changement d’état, la température est constante : on dit que cela forme un palier de température.
Pression et température
Plus on monte en altitude, plus la pression atmosphérique baisse. L’eau bout alors à une température inférieure à 100°C. Par exemple, au sommet du Mont-Blanc, l’eau bout à 83°C. Dans une cocotte-minute, la pression étant plus forte, l’eau bout à environ 120°. On appelle pression atmosphérique la force exercée par les constituants de l'air sur les éléments qui l'entourent. Par exemple, la pression atmosphérique exerce une pression sur les Hommes à la surface de la Terre. La pression atmosphérique est mesurée en Pascal d'après le Système International. Il existe un lien entre altitude et pression. En effet, plus l'altitude augmente et plus la pression diminue. On considère que la pression diminue d'un facteur 10 tous les 16 km de plus. On mesure la pression atmosphérique à l'aide de plusieurs appareils tels que le baromètre, l'altimètre ou encore l'hypsomètre. Son unité est le Pascal dans le Système International, même si on utilise couramment le bar. En moyenne, la pression atmosphérique de base est de 1013 hPa au niveau de la mer soit 1,013 bar.
Lois sur les gaz parfaits
La loi de Boyle-Mariotte
Cette loi établie par deux physiciens concerne la thermodynamique des gaz parfaits. C'est le physicien botaniste Edme Mariotte, un abbé français ayant vécu de 1620 à 1684 et le physicien chimiste Robert Boyle, un itrlandais ayant vécu de 1627 à 1691 qui ont énoncé cette loi sur la pression et les volumes des gaz parfaits. Cette loi indique que pour garder une température constante durant une augmentation de la pression d'un gaz, il faut que le volume diminue. Cette loi est également vraie à l'inverse, ce qui signifie que pour baisser la pression d'un gaz en gardant la même température, il faut augmenter le volume.
La loi de Charles
Cette loi a été mise au jour par Jacques Charles, un célèbre physicien, chimiste et inventeur français ayant vécu entre 1746 et 1823, et qui fut aussi reconnu comme ayant été le premier homme à avoir fait voler un ballon à gaz rempli d'hydrogène. Cette loi explique que quand la pression d'un gaz reste constante, le volume d'une quantité donnée d'un gaz varie proportionnellement à la température absolue. Voici la formule énoncée par la loi de Charles ; 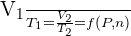 où f (P,n) est une fonction qui dépend du volume V et de la quantité de matière n qui restent constants dans les états 1 et 2.
où f (P,n) est une fonction qui dépend du volume V et de la quantité de matière n qui restent constants dans les états 1 et 2.
La loi de Gay-Lussac
Cette loi de thermodynamique, elle aussi appliquée au gaz parfaits à été énoncée par Louis Gay-Lussac, un physicien chimiste français ayant vécu de 1778 à 1850. Il a effectué de nombreux travaux sur les gaz et leurs propriétés. Cette loi évoque qu'à volume constant la pression de deux gaz parfaits est liée à la température absolue mesurée en Kelvin. Voici la relation énoncée par cette loi :  où V volume constant, P pression du gaz en Pascal et T température du gaz en Kelvin.
où V volume constant, P pression du gaz en Pascal et T température du gaz en Kelvin.
La loi d'Avogadro
La loi d'Avogadro, aussi appelée loi d'Ampère ou loi d'Avogadro-Ampère, cette loi de thermodynamique en rapport avec les gaz parfaits fut énoncée en 1811 par Amedeo Avogadro, une célèbre physicien et chimiste originaire d'Italie ayant vécu entre 1776 et 1856. Egalement connu pour avoir donné son nom au nombre d'Avogadro qui sert à calculer le nombre d'éléments contenus dans une mole, il a énoncé cette loi selon laquelle pour deux gaz parfaits différents, le même volume contient forcément le même nombre de molécules si les conditions de pression et de température sont les mêmes, ce qui signifie également qu'à mêmes conditions de température et de pression, tous les gaz parfaits auront le même volume molaire. D'après cette loi, dans des conditions habituelles de pression à 1 bar et avec 20°C, une mole de gaz parfait occupera 24 L. Voici la formule exprimée pour deux gaz parfaits 1 et 2 :  avec V, volume de gaz et n, nombre de molécules de gaz.
avec V, volume de gaz et n, nombre de molécules de gaz.
La loi de Dalton
Aussi appelée loi des pressions partielles, la loi de Dalton explique que la pression dans un mélange de gaz parfaits est égale à la somme des pressions partielles de tous les gaz qui constituent le mélange. John Dalton était un chimiste et physicien anglais ayant vécu de 1766 à 1844 qui a effectué de nombreuses recherches sur la physique mais tout particulièrement sur la maladie qui porte son nom : le daltonisme. Cette loi peut donc s'écrire comme ceci : 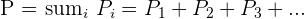
Loi générale
Ces 5 lois sur les gaz parfaits constituent la loi générale des gaz parfaits qui s'énonce comme ceci : 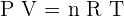 Dans cette équation, on retrouve P, la pression du gaz ; V, le volume du gaz ; n la quantité de gaz exprimé en nombre de moles et R la constante des gaz parfaits qui représente 8,314462 1 J mol−1 K−1.
Dans cette équation, on retrouve P, la pression du gaz ; V, le volume du gaz ; n la quantité de gaz exprimé en nombre de moles et R la constante des gaz parfaits qui représente 8,314462 1 J mol−1 K−1.
Les états de l’eau

L’eau pure, dans des conditions normales de pression, est :
- Liquide si sa température est supérieure à 0°C.
- Solide si sa température est inférieure à 0°C.
Au cours de la solidification et de la fusion de l’eau pure, la température est constante et égale à 0°C.
L'eau solide
L'eau atteint son état solide lorsque la température atteint ou descend les 0° C. Les molécules adoptent donc une structure cristalline.
L'eau liquide
On peut trouver de l'eau liquides dans les conditions climatiques habituelles de nos environnements de vie. En effet, sous pression atmosphérique normale de 1 bar et entre 0° C et 100° C, l'eau prend sa forme liquide. Elle adopte alors uns structure plus désordonnée et prends moins de place. C'est pourquoi l'eau gelée occupe plus de place que l'eau liquide.
L'eau gazeuse
La majorité de l'eau gazeuse est celle que nous respirons dans l'air. A pression normale de 1 bar et une fois passé la barre des 100° C, l'eau devient gazeuse et l'on parle alors de vapeur d'eau. C'est aussi l'état de l'eau qui s'évapore (au dessus des lacs, rivières ou océans). Les molécules d'eau sont dans leur état le plus agité lorsqu'elles sont gazeuses. L'attraction terrestre s'exerce alors moins dessus et permet au gaz de s'expanser.
Masse, volume et changement d’état
Au cours d’un changement d’état, la masse se conserve, mais le volume varie. Par exemple, en remplissant une bouteille d’eau puis en la congelant, sa masse ne change pas, mais la bouteille éclate : le volume augmente. La matière existe sous différents états : solide, liquide et gazeux. On appelle changement d'état la transformation physique qui correspond au passage d'un état à un autre. La température d'ébullition d'une espèce chimique est la température à laquelle cette espèce passe de l'état liquide à l'état gazeux, lors, de la vaporisation. Sous une pression donnée, l’ébullition d'un corps pur se fait à une température constante, caractéristique de ce corps.
Solubilité
On appelle solvant une espèce chimique dans laquelle on peut dissoudre d'autres espèces chimique, appelées solutés. L'ensemble ainsi formé s'appelle une solution. La solubilité d'une espèce chimique est la masse maximale (en g) de cette espèce que l'on peut dissoudre dans un litre de solution. Elle s'exprime en gramme par litre (g.L1).
Masse volumique
Les masses volumiques sont souvent exprimées dans d'autre unités que celles du Système international, comme par exemple le gramme par litre (g.L^-1) ou le kilogramme par litre (kg.L^-1). Elles représentent la masse de principe actif dans un volume donnée de médicament.
Résumer avec l'IA :























Si vous désirez une aide personnalisée, contactez dès maintenant l’un de nos professeurs !
merci beaucoup et j’apprécie
Bonjour,
Bravo pour votre article. Il me semble en revanche que le sens de la flèche « Condensation solide » n’est pas bon.
Cordialement
Bonjour Jérémie, merci pour cette remarque. Nous allons remplacer l’image erronée ! Bonne journée.
bien