Chapitres

Mole et quantité de matière
La mole est une unité de quantité de matière.
La quantité de matière se note n et s'exprime en mole de symbole mol.
Le nombre d'entités élémentaires contenues dans une mole est appelé Constante d'Avogadro, noté Na.
Il faut savoir que la valeur du nombre d'Avogadro a évolué au court du temps :
- Avant le 20 Mai 2019, le nombre d'Avogadro, et donc la mole, était défini comme correspondant au nombre d'atome de carbone dans 12 grammes (donc 10-3 kg) de carbone 12. On avait alors : NA = 6,022 140 857 . 1023 mol−1.
- Or, depuis le 20 Mai 2019, le kilogramme a été redéfini. Ainsi, on fit le choix de définir le nombre d'Avogadro comme étant une constante fixée par convention. Aujourd'hui, la valeur du nombre d'Avogadro est donc : NA = 6,022 140 76 . 1023 mol−1
Il y a proportionnalité entre le nombre N d'entités élémentaires dans un échantillon et sa quantité de matière n :
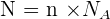
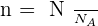
De façon plus générale, la mole, de symbole mol, correspond à l'une des unités de base du système international et est principalement utilisée en physique et en chimie suite à son adoption en 1971.
Plus précisément, la mole correspond à une quantité de matière d'un système contenant, et ce de façon exacte, 6,022 140 76 . 1023 entités élémentaires ce qui pourrait correspondre, en terme d'ordre de grandeur, à la quantité de grain de pop-corn nécessaire pour recouvrir la surface totale des Etats-Unis d'une couche uniforme et épaisse de 14 km de grains.

La masse molaire
La masse d'une mole d'atomes est appelée masse molaire atomique, noté M et d'unité g / mol. En chimie, on ne compte pas en nombre d'ions ou d'atomes mais en nombre de paquets, un paquet s'appelle une mole (mol). Une mole contient 6,02 . 1023 entités.
Le nombre de masse d’un atome correspond au nombre de nucléons qu’il contient. Il s’agit donc de la somme du nombre de protons et du nombre de protons qui constituent le noyau de l’atome.
La masse molaire correspond aussi au nombre de nucléons dans le noyau. A = 59, signifie qu'il y a 56 nucléons dans le noyaux (et 59 grammes dans une mole).
Dans le tableau périodique, la masse molaire est souvent différente de A à cause des isotopes.
Des isotopes sont des atomes qui possèdent le même nombre de protons mais un nombre différent de neutrons.
Concentration molaire et quantité de matière : la dilution
La dilution correspond à un procédé qui consiste en l'obtention d'une solution finale qui présentera une concentration inférieure à la concentration de la solution de départ.
Il est alors possible de procéder à cela grâce à un ajout de solvant ou encore en prélevant une partie de la solution puis de compléter jusqu'à atteindre le volume souhaité avec du solvant. Il est alors possible de caractériser une dilution par son taux de dilution. Mais pour cela, il est nécessaire de présupposer que le corps dilué est soluble dans le solvant qui est utilisé.
Dilution par ajout de solvant
On note la concentration d'une solution C et il est possible de la calculer avec la formule suivante : 
Avec :
- C la concentration molaire. Cette unité s'exprime en mol.L-1 ;
- n la quantité de matière du soluté en solution. Cette unité s'exprime en mol ;
- Et V le volume de solvant. Cette unité s'exprime en L.
Ainsi, si on procède à une dilution par ajout de solvant, la solution initiale et la solution finale contiennent autant de quantité de soluté. Cela signifie alors que ninitiale = nfinale .
On a alors les relations suivantes qui se dégagent :
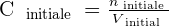

On peut déduire de ces relations le rapport suivant :
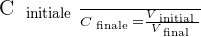
Taux de dilution
Il est possible d'exprimer le taux de dilution avec la relation suivante :
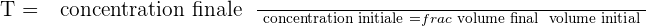
Il est important de savoir que le taux de dilution, noté T, est une grandeur sans unité et qui présente obligatoirement une valeur positive et inférieure à 1.
Quant au taux de dilutions successives, il correspond au produit des taux de dilution de chaque dilution.
Exemple
Si on procède à une dilution à 3 % puis à 5 %, on a T qui est égal à :

La dilution dans la vie de tous les jours : l'homéopathie
L'homéopathie correspond à une pratique pseudo-scientifique de médecine alternative qui a été inventée en 1796 par Samuel Hahnemann.
Cette pratique repose essentiellement sur le principe qu'il est possible de soigner un patient en diluant très fortement des substances qui, lorsqu'elles sont concentrées, pourraient provoquer des symptômes assez similaires à ceux que le patient rencontre.
Or, au delà d'un certain nombre de dilutions, les remèdes se basant sur l'homéopathie sont totalement dépourvus de tout principe actif.
Afin de mettre au point un remède homéopathique, il est nécessaire d'utiliser la technique de dilutions infinitésimales. Ce principe consiste à diminuer la toxicité des substances choisies dans la composition du remède par application du principe de similitude. Suite à cela, il est nécessaire d'agiter très fortement les préparations. Ainsi, après chaque dilution, la préparation est secouée de façon énergique manuellement ou mécaniquement. Cela permettrait de conserver les effets pharmacologiques du principe malgré des dilutions importantes.
La mémoire de l'eau
Pour expliquer cette méthode, Jacques Benveniste, en 1987, mettra au point l'hypothèse de la mémoire de l'eau. Cette hypothèse reposerait sur la possibilité que l'eau garderait en mémoire les propriétés de la substances précédemment diluées même lorsque ces substances sont absente sous la forme d'une empreinte électromagnétique de la molécule.
Cependant, cette hypothèse est considérée comme scientifiquement invraisemblable, et les précédentes démonstrations de cette hypothèse ne furent nullement convaincantes car truquées ou biaisées par la présence d'artefacts de manipulations.
Rappels de base pour un exercice réussi
Les conventions d'écriture concernant les unités comme la mole
Par convention, les noms d'unités sont des noms communs on les écrit alors en minuscules : par exemple, on écrit « kelvin » et non « Kelvin », « ampère » et non « Ampère ».
Pourtant, ces unités ont pour origine les noms propres des savants qui les ont inventées. De plus, puisque ces unités sont des noms communs, il peuvent prendre la marque du pluriel, (par exemple, on écrit un volt mais aussi deux volts).
Cependant, les symboles prennent une majuscule (sauf convention contraire) si le nom de ces unités dérivent du nom d'une personne.
Par exemple, on écrit "V" pour volt, provenant d'Alessandro Volta, "A" pour ampère provenant d'André-Marie Ampère et "Pa" pour pascal provenant de Blaise Pascal. Si le symbole ne dérive pas d'un nom propre, le symbole commence par une minuscule. C'est le cas des mètres qui s'écrit "m" mais aussi pour la mole qui s'écrit "mol".
Cependant, il peut exister quelques exceptions adoptées lors des conférences générales des poids et mesures. Ces exceptions ont été adoptées pour éviter toute confusion, c'est le cas du litre qui se symbolise par "L". Il en a été décidé ainsi pour éviter tout confusion avec la lettre "l" et le chiffre "1".
L'unité du degré Celsius n'est pas une exception. Il ne faut pas oublier que son écriture correcte est le "degré Celsius" qui se symbolise par "°C". Les caractères ° et C sont indissociables puisque l'unité commence par le degré et que Celsius est un qualificatif. En effet, il existe différents degrés différents comme le degré Fahrenheit.
Le lien entre les unités et la logique scientifique
La dimension d'une grandeur traduit la nature physique de cette grandeur. Si deux grandeurs présentent la même dimension, alors elles sont dites homogènes. Bien évidemment, seule la comparaison de deux valeurs de grandeurs physiques homogènes a un sens !
Par exemple, il est insensé de comparer une énergie à une masse puisque ce sont des grandeurs de natures différentes.
Les unités permettent donc de quantifier la mesure d'une grandeur physique.
Le système international et les grandeurs usuelles

L'ensemble des unités associées aux dimensions fondamentales constitue le système international d'unités. Il s'agit du système MksA (mètre, kilogramme, seconde, ampère), mais le kelvin, le mole et le candela font aussi partie de ce système. Ces unités sont appelées unités légales. Elles sont universelles et connues de par le monde entier.
Il est important de savoir que toutes les autres dimensions se déduisent de ces sept dimensions fondamentales par produit ou division de ces dimensions.
Dans certains sujets d'exercices, les grandeurs ne sont pas exprimées dans le système international mais avec des grandeurs usuelles. Il est facile de les comprendre et elles sont parfois utilisées dans la vie de tous les jours, mais il est essentiel de toujours effectuer les calculs avec les grandeurs exprimées dans l'unité internationale pour éviter les erreurs.
Par exemple, la pression est souvent exprimée en bar. Or, dans le système international, la pression s'exprime en pascal !
Exercice 1
Dans une synthèse organique, on fait réagir du benzaldéhyde en présence de potasse. Pour cela, le protocole indique d'introduire n = 0,450 mol de benzaldéhyde (qui est un liquide) de formule brute C7H6O.
- Calculer le nombre N de molécules présentes dans les 0,450 mol de benzaldéhyde.
- Calculer la masse molaire M du benzaldéhyde.
- En déduire la masse m de benzaldéhyde à introduire. Comment procédera-t-on pour la mesure?
- Le flacon de benzaldéhyde indique sa densité d = 1,05. Calculer le volume V de benzaldéhyde qu'il faut verser dans le ballon.
- En déduire le volume molaire Vm du benzaldéhyde.
Donnée: M(C) = 12,0 g.mol-1 M(H) = 1,0 g.mol-1 M(O) =16,0 g.mol-1
Exercice 2

Une boite de comprimés effervescents d'aspirine (acide acétylsalicylique) comporte l'information suivante :
COMPOSITION: Acide acétylsalicylique 500 mg, excipient q.s.p. un comprimé en hydrogénocarbonate de sodium. Le gaz libéré lors de l'effervescence d'un comprimé est du dioxyde de carbone de formule moléculaire CO2.
La formule moléculaire de l'acide acétylsalicylique est C9H8O4 : donner sa masse molaire moléculaire.
- Calculer la quantité de matière n d'acide acétylsalicylique présente dans le comprimé.
- Quel est le nombre réel N de molécule d'acide acétylsalicylique correspondant ?
Sur un plateau d'une balance, on pose deux comprimés ainsi qu'un bécher rempli d'eau.
La balance affiche une masse totale, noté mi = 164,87 g. On introduit les comprimés dans l'eau du bécher : la dissolution de l'excipient des comprimés provoque une effervescence; la valeur de la masse affichée par la balance diminue rapidement et se stabilise à la valeur mf = 164,17 g.
- Quelle est la masse de dioxyde de carbone CO2 libérée par la dissolution des deux comprimés ?
- Calculer la quantité de matière de CO2 gazeux libéré lors de l'effervescence.
- Quel est le volume de CO2 gazeux libéré, dans le cas où la pression atmosphérique est normale et la température 25° C ?
Données: M(C) = 12,0 g.mol-1 M(H) = 1,0 g.mol-1 M(O) = 16,0 g.mol-1
Na = 6,02 x 1023 mol-1 à 25°C et pression normale 1,013 x 105 Pa , Vm = 24,5 L.mol-1
Exercice 3
Pour recouvrir la charpente de la statut de la liberté dans le port de New York, on utilise 9,08 x 104 kg de plaques de cuivre. Quelle quantité de cuivre (exprimée en mol) cela représente-t-il ?
Correction Exercice 1
1- On cherche combien de molécules sont présentes dans n.
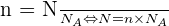
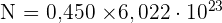
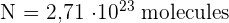
2- 


3- 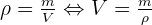

4- 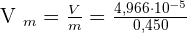
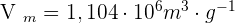
Correction Exercice 2
1- 
2- 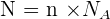 ou
ou 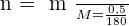
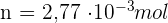
Donc 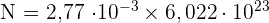
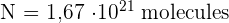
3- 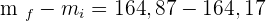

4- 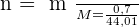
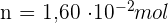
5- 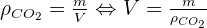
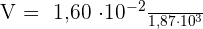
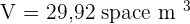
Correction Exercice 3

























Si vous désirez une aide personnalisée, contactez dès maintenant l’un de nos professeurs !
J’ai des doutes avec votre correction sinon merci pour les exercices!
Bonjour , je pense qu’il y a une faute concernant l’exercice 3. Entre l’énoncé et la correction une incohérence est présente :
– dans l’énoncé il est écrit : 9.08×10 ( puissance 4) hors dans la correction il est écrit : 9.08×10 ( puissance 7) ?
Merci de votre compréhension
Je pense en effet qu’il y a une erreur, en effet il y a marquer puissance 7 car on passe des kilos aux grammes donc là ok mais ce n’est pas logique d’obtenir puissance 7 on devrait avoir comme résultat 1,43 x 10 exposant 6